Kalcium-karbonát (original) (raw)
A Wikipédiából, a szabad enciklopédiából
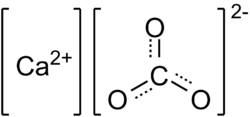
| Kalcium-karbonát | |
|---|---|
 |
|
 |
|
 |
|
| IUPAC-név | kalcium-karbonát |
| Más nevek | mészkő, calcii carbonas, szénsavas mész |
| Kémiai azonosítók | |
| CAS-szám | 471-34-1 |
| PubChem | 10112 |
| ChemSpider | 9708 |
| EINECS-szám | 207-439-9 |
| DrugBank | DB06724 |
| KEGG | C08129 |
| ChEBI | 3311 |
| RTECS szám | FF9335000 |
| ATC kód | , A02AC01, A12AA04 |
| Gyógyszer szabadnév | calcium carbonate |
| InChIKey | VTYYLEPIZMXCLO-UHFFFAOYSA-L |
| UNII | H0G9379FGK |
| ChEMBL | CHEMBL1200539 |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | CaCO3 |
| Moláris tömeg | 100,09 g/mol |
| Megjelenés | fehér por, illetve fehér rögök |
| Halmazállapot | szilárd |
| Sűrűség | 2,93 g/cm³ |
| Olvadáspont | 825 °C (bomlik) |
| Forráspont | olvadáspont közelében bomlik |
| Oldhatóság (vízben) | 0,014 g/l (0°C, 100 kPa) |
| Kristályszerkezet | |
| Kristályszerkezet | tetraéder |
| Termokémia | |
| Std. képződési entalpia Δf_H_ |
−1207 kJ/mol |
| Standard moláris entrópia S |
93 J/(mol·K) |
| Veszélyek | |
| EU osztályozás | nincsenek veszélyességi szimbólumok[1] |
| R mondatok | (nincs)[1] |
| S mondatok | (nincs)[1] |
| Lobbanáspont | nem gyúlékony |
| Rokon vegyületek | |
| Azonos kation | a kalcium vegyületei |
| Azonos anion | karbonátok |
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. |
A kalcium-karbonát (mészkő, szénsavas mész, CaCO3) a karbonátok közé tartozó szervetlen vegyület. Különböző ásványai számos kőzet, köztük a mészkő fő összetevői. A kalcium-karbonát a puhatestűek és a gerincesek vázának fő alkotórésze. A vezetékes vízből kiválva a magnézium-karbonáttal együtt alkotja a vízkövet. Az építkezésekhez szükséges habarcs és cement alapanyaga. Az orvoslásban savmegkötőként és kalciumionok bevitelére használják. A VIII. Magyar Gyógyszerkönyvben calcii carbonas néven hivatalos.
Az IUPAC szerinti magyar kémiai nevezéktanban kalcium-karbonát a neve. A nyelvújításkori, mára elavult kémiai nevezéktanban szénsavanyos mész nevet használták.
A kalcium-karbonát az építkezéseken használt habarcs és cement előállításának alapanyaga. Mészkő formájában építőanyagként is alkalmazzák, különösen jól bevált a nedves vidékeken.[2] A kalcium-karbonátot az orvoslásban savmegkötőként és kalciumionok bevitelére használják.[3]
A kalcium-karbonátból égetett meszet, majd oltott meszet állítanak elő, melyből többek között habarcsot készítenek, amit az építkezéseken kötőanyagként használnak. Az eljárás során a kalcium-karbonátot hevítik, melynek hatására 885 °C felett szén-dioxid távozik belőle, és kalcium-oxiddá alakul. A folyamatot mészégetésnek, a kalcium-oxidot égetett mésznek nevezik.
C a C O 3 → C a O + C O 2 {\displaystyle \mathrm {CaCO_{3}\rightarrow CaO+CO_{2}} \!}
A kalcium-oxid vízben való oldásával, a mészoltással kalcium-hidroxid oldatot, oltott meszet nyernek. Az oltott meszet homokkal keverik, így kapják a habarcsot.
C a O + H 2 O → C a 2 + + 2 O H − {\displaystyle \mathrm {CaO+H_{2}O\rightarrow Ca^{2+}+2\ OH^{-}} \!}
A habarcsot kötőanyagként alkalmazzák, mivel levegőn állva lassan "megköt", karbonátosodik.
C a ( O H ) 2 + C O 2 → C a C O 3 + H 2 O {\displaystyle \mathrm {Ca(OH)_{2}+CO_{2}\rightarrow CaCO_{3}+H_{2}O} \!}
Klinkercement, a cementgyártás közbülső terméke
Fő szócikk: Cement
A mészkő kőzetben lévő kalcium-karbonátból agyag hozzáadásával ún. portlandcementet, másképpen szilikátcementet készítenek. A mészkő és agyag keverékét megőrlik, majd kb. 1500 °C-ra hevítik. A kiégetéssel kapott szürkészöld színű rögöket, az ún. klinkercementet porrá őrlik. Az így kapott portlandcement különböző ásványok keveréke, tulajdonságai az összetevők arányától függenek.
A keverék főbb elemei:
- 3 CaO · SiO2 (trikalcium-szilikát)
- 2 CaO · SiO2 (dikalcium-szilikát)
- 4 CaO · Al2O3 · Fe2O3 (tetrakalcium-aluminát-ferrit)
- 3 CaO · Al2O3 (trikalcium-aluminát)
E négy összetevő víz hatására igen kemény, stabil vegyületté alakul át. Ez a folyamat a cement megkötése.
A kalcium-karbonátból bizonyos segédanyagokkal olyan speciális műtrágyát készítettek, mely a növényeken fehér bevonatot képez, ezáltal alkalmas azok napégés elleni védelmére.
Lásd még: Mészkő, Dolomit, Kalcit
A kalcium-karbonát számos ásvány (kalcit, aragonit, dolomit, vaterit vagy μ-CaCO3) és kőzet alapvető alkotója. Kőzetei közül az üledékes kőzetek a gyakoribbak.
Legismertebb kőzete a több, mint 90% kalcium-karbonátot tartalmazó mészkő. A kréta a mészkő különleges változata. Az édesvizekből kicsapódó mésztufától és travertinótól jól megkülönböztethető a tengervízből kiváló, kevésbé porózus, tömörebb diagenizált mészkő.
A dolomit kőzet több, mint 90%-a dolomit ásvány, amely kalcium-magnézium-karbonátból (CaCO3*MgCO3) áll.
Az átmeneti karbonátos kőzetek összetétele a mészkő (illetve a dolomit) és az agyag közötti.
Szintén meglehetősen ismert, de jóval kevésbé gyakori a szinte tiszta kalcium-karbonátból álló, és a mészkő metamorfózisával keletkező átalakult kőzet, a márvány.
A kalcium-karbonát ásványai (főleg a kalcit) ezenkívül előfordulnak számos telérkőzetben és egyéb hidrotermális képződményben. Aktívan részt vesznek a talajok meszesedésében – ez a folyamat a Kárpát-medence középső részén általános. Kalcium-karbonát ásványokból (kalcit, aragonit) áll a barlangi képződmények többsége.
A jórészt karbonátásványokból (egyebek közt kalcitból is) álló magmás kőzetek a karbonatitok. A Föld egyetlen, működő karbonatitvulkánja a Kelet-Afrikai árokban (Kenyában, a Turkana-tótól délre) található Ol Doinyo Lengai.
A tojáshéj kb. 95%-a kalcium-karbonát.[4] Kalcium-karbonátot tartalmaz a puhatestűek[5] váza és a gerincesek[_forrás?_] csontos váza.
A kalcium-karbonát fehér, kristályos, szobahőmérsékleten szilárd vegyület. Fizikai tulajdonságai jelentősen függenek kristályszerkezetétől.
Lásd még: Karbonát
Vízben igen kis mértékben, savakban jól oldódik. Szénsavas vízben oldható, ez a reakció felelős a mészkőbarlangok és a cseppkövek kialakulásáért is.[6]
C a C O 3 + H 2 C O 3 ⇌ C a 2 + + 2 H C O 3 − {\displaystyle \mathrm {CaCO_{3}+H_{2}CO_{3}\rightleftharpoons Ca^{2+}+2\ HCO_{3}^{-}} \!}
A vízkő kalcium-karbonátból és magnézium-karbonátból áll
A vízben oldott kalcium- és hidrokarbonátionok kalcium-karbonátként kiválhatnak. A kivált kalcium-karbonát a magnézium-karbonáttal együtt alkotja a vízkövet.
C a 2 + + 2 H C O 3 − ⇌ C a C O 3 _ + C O 2 + H 2 O {\displaystyle \mathrm {Ca^{2+}+2\ HCO_{3}^{-}\rightleftharpoons {\underline {CaCO_{3}}}+CO_{2}+H_{2}O} \!}
Ha egy erős savat, például sósavat cseppentünk olyan kőzetre, ami karbonátot (esetünkben kalcium-karbonátot) tartalmaz, pezsgést tapasztalunk a fejlődő szén-dioxid miatt.
2 H + + C a C O 3 → C a 2 + + C O 2 + H 2 O {\displaystyle \mathrm {2\ H^{+}+CaCO_{3}\rightarrow Ca^{2+}+CO_{2}+H_{2}O} \!}
A fejlődő szén-dioxid a meszes vizet, vagyis a kalcium-hidroxid vizes oldatát megzavarosítja.
C O 2 + C a 2 + + 2 O H − → C a C O 3 _ + H 2 O {\displaystyle \mathrm {CO_{2}+Ca^{2+}+2\ OH^{-}\rightarrow {\underline {CaCO_{3}}}+H_{2}O} \!}
- Balogh K. et al.: Szedimentológia I–III. (Akadémiai Kiadó, Budapest, 1991.)
- Bodonyi Ferenc: Kémiai összefoglaló (Műszaki Könyvkiadó, Budapest, 1987., p. 327, 337; ISBN 963-10-7229-0)
- Molnár B., 1980.: Hiperszalin tavi dolomitképződés a Duna-Tisza közén. (Földtani Közlöny 110., p. 45–64; HU ISSN 0015-542X)
- www.malagrow.hu
- ↑ a b c A kalcium-karbonát vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. (JavaScript szükséges) (angolul)
- ↑ Limestone Rocks Archiválva 2008. május 13-i dátummal a Wayback Machine-ben (The Franklin Institute)
- ↑ Újra jóízűen enni - HáziPatika.com
- ↑ Látványos kémiai kísérletek Archiválva 2009. április 8-i dátummal a Wayback Machine-ben (a Szegedi Tudományegyetem Orvosi Vegytani Intézete Archiválva 2008. március 15-i dátummal a Wayback Machine-ben)
- ↑ Geokronológiai segédanyag Archiválva 2007. július 9-i dátummal a Wayback Machine-ben (a Pécsi Tudományegyetem Földrajzi Intézete)
- ↑ https://tudasbazis.sulinet.hu/hu/termeszettudomanyok/kemia/szervetlen-kemia/alkali-es-alkalifemsok/a-meszko-es-a-dolomit
 **Kémiaportál**• összefoglaló, színes tartalomajánló lap
**Kémiaportál**• összefoglaló, színes tartalomajánló lap








