Гидрокарбонаты | это... Что такое Гидрокарбонаты? (original) (raw)

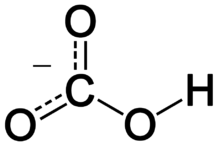
Модель иона гидрокарбоната HCO3−

Гидрокарбонаты — кислые соли угольной кислоты H2CO3. Формула аниона: HCO3-. Устаревшие названия гидрокарбонатов: кислый углекислый, или двууглекислый.
Гидрокарбонаты щелочных металлов в воде растворимы. Также в воде хорошо растворимы гидрокарбонаты щелочноземельных металлов, в отличие от карбонатов.
Содержание
- 1 Получение
- 2 Химические свойства
- 3 Применение
- 4 Физиологическое действие
- 5 Литература
- 6 Примечания
- 7 См. также
Получение
- Гидрокарбонаты образуются при длительном пропускании CO2 через раствор, содержащий карбонат:

- А пищевую соду получают по так называемому аммиачно-хлоридному способу:

Гидрокарбонат натрия плохо растворим в холодной воде, поэтому его можно отделить от хлорида аммония фильтрованием.
Химические свойства
- При нагревании гидрокарбонаты разлагаются на соответствующий карбонат, воду и углекислый газ:

- Гидролиз гидрокарбонат-иона происходит по схеме:

В итоге раствор гидрокарбонатов имеет щелочную реакцию.
- Реагирует с щелочами:

- С кислотами:

Применение
Гидрокарбонат натрия (сода) используется в производстве искусственных минеральных вод и заправки огнетушителей, в кондитерском деле и хлебопечении, в быту, в медицине.
Гидрокарбонаты кальция и магния Са(НСО3)2, Mg(НСО3)2 обусловливает временную жёсткость воды[1].
Физиологическое действие
В организме гидрокарбонаты являются буферными веществами, регулирующими постоянство реакции крови[1].
Литература
- Кнунянц И. Л. и др. т.3 Мед-Пол // Химическая энциклопедия. — М.: Большая Российская Энциклопедия, 1992. — 639 с. — 50 000 экз. — ISBN 5-85270-039-8
- Ф.Н. Капуцкий, В.Ф.Тикавый Пособие по химии для поступающих в вузы. — Минск: Выш. школа, 1979. — С. 384.
- Г.П.Хомченко Химия для поступающих в вузы. — М.: Высшая школа, 1994. — С. 447.
Примечания
См. также
 Оксиды углерода Оксиды углерода |
||
|---|---|---|
| Оксиды | CO2 · CO |  |
| Экзотические оксиды | Карбонилы металлов · Угольная кислота · Гидрокарбонаты · Карбонаты · Дикарбонаты · Трикарбонаты |