1,2-дихлорэтан | это... Что такое 1,2-дихлорэтан? (original) (raw)
У этого термина существуют и другие значения, см. Дихлорэтан.
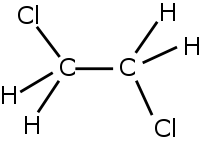
| 1,2-дихлорэтан | |
|---|---|
 |
|
 |
|
| Общие | |
| Систематическое наименование | 1,2-дихлорэтан |
| Химическая формула | C2H4Cl2 |
| Физические свойства | |
| Состояние (ст. усл.) | жидкость |
| Молярная масса | 98,96 г/моль |
| Плотность | 1,253 г/см³ |
| Термические свойства | |
| Температура плавления | -35 °C |
| Температура кипения | 83,5–84,0 °C |
| Удельная теплота испарения | 32,024 Дж/кг |
| Удельная теплота плавления | 8,837 Дж/кг |
| Химические свойства | |
| Растворимость в воде | 0,87 г/100 мл |
| Структура | |
| Дипольный момент | 1,80 Д |
| Классификация | |
| Рег. номер CAS | 107-06-2 |
| SMILES | ClCCCl |
| Безопасность | |
| Токсичность | очень токсично |
| R-фразы | R10, R16, R18, R33, R36/37/38, R39/26/28, R44, R45, R46, R48/21, R51/53, R55, R56, R57, R67 |
| NFPA 704 |  3 4 1 3 4 1 |
1,2-дихлорэтан ClCH2—СН2Cl — хлорорганическое соединение, прозрачная бесцветная жидкость с сильным запахом похожим на запах хлороформа, практически не растворимая в воде. Хороший растворитель. Легко испаряется, образует азеотроп с водой (71, 5°С, 82,9 вес % дихлорэтана). 1,2-дихлорэтан относится к токсичным веществам.
Содержание
Производство
Каждый год в США, Западной Европе и Японии вместе взятых производится более 17,5 млн тонн дихлорэтана.[1] Основным методом получения является катализируемая хлоридом железа (III) реакция присоединения хлора к этилену.

Также существует метод, основанный на реакции этилена с хлороводородом и кислородом в присутствии катализатора на основе хлорида меди (II):

В принципе, он может также быть получен хлорированием этана или из этанола.
Химические свойства
При нагревании с водой, раствором соды или суспензией гашёной извести, дихлорэтан образует этиленгликоль;

действием щёлочи или пиролизом превращается в хлористый винил. При нагревании дихлорэтана с аммиаком под давлением даёт этилендиамин

с цианистым натрием дихлорэтан образует динитрил янтарной кислоты.

При нагревании с растворами полисульфидов натрия дихлорэтан образует каучукоподобное вещество - тиокол.

Реагирует с алюминием, а во влажном состоянии с цинком и железом.
Применение
Получение винилхлорида
Примерно 80 % производимого в мире дихлорэтана используется для получения винилхлорида, важного исходного соединения для синтеза полимерных материалов, в частности — поливинилхлорида.

Очистка в лаборатории
Промывают концетрированной серной кислотой, затем водой и перегоняют над пентаоксидом фосфора.
Другие применения
Используется в органическом синтезе в качестве прекурсора или растворителя, для извлечения жиров и алкалоидов, как инсектицид для обеззараживания зерна, зернохранилищ и почвы виноградников. Используется моделистами для склейки некоторых пластмасс (например оргстекла). Применялся в качестве антидетонационной присадки в топливо.
Безопасность
Дихлорэтан — сильное наркотическое средство, канцероген, при приёме внутрь или вдыхании паров вызывает отравление. Допустимая концентрация паров в воздухе производственных помещений 0, 01%. Дихлорэтан относят к легко воспламеняющимся жидкостям[2]. Пределы взрывчатости в воздухе 6, 20 — 15, 90 об. %. Взрывается при контакте с натрием. Экологически опасен и имеет период полураспада 50 лет. В качестве заменителя предлагается диоксан и толуол.
Примечания
- ↑ J.A. Field & R. Sierra-Alvarez (2004). «Biodegradability of chlorinated solvents and related chlorinated aliphatic compounds». Rev. Environ. Sci. Biotechnol. 3: 185–254. DOI:10.1007/s11157-004-4733-8.
- ↑ ГОСТ 1942-86: 1,2-Дихлорэтан технический. Технические условия. Проверено 25 декабря 2012.
Ссылки
 |
|---|