Прионы | это... Что такое Прионы? (original) (raw)
| Прионы | |
|---|---|
| МКБ-10 | A81 |
| МКБ-9 | 046046 |
Не путать с гипотетическими элементарными частицами — преонами
Прио́ны (от англ. proteinaceous infectious particles — белковые заразные частицы) — особый класс инфекционных агентов, чисто белковых, не содержащих нуклеиновых кислот, вызывающих тяжёлые заболевания центральной нервной системы у человека и ряда высших животных (т. н. «медленные инфекции»).
Прионный белок, обладающий аномальной трёхмерной структурой, способен прямо катализировать структурное превращение гомологичного ему нормального клеточного белка в себе подобный (прионный), присоединяясь к белку-мишени и изменяя его конформацию. Как правило, прионное состояние белка характеризуется переходом α-спиралей белка в β-слои. Прионы — единственные инфекционные агенты, размножение которых происходит без участия нуклеиновых кислот.
Содержание
- 1 История
- 2 Свойства молекул
- 3 Молекулярные основы патогенеза
- 4 Классификация
- 5 Этиология
- 6 Пути заражения
- 7 Прионы и медицинские инструменты
- 8 Прионные заболевания человека
- 9 Потенциальная опасность для человека
- 10 Исследования прионов дрожжей и других микромицетов
- 11 Критика
- 12 См. также
- 13 Примечания
- 14 Литература
- 15 Источники
- 16 Ссылки
История
 |
В этом разделе не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена.Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники.Эта отметка установлена 12 мая 2011. |
|---|
Во второй половине XX века врачи столкнулись с необычным заболеванием человека — постепенно прогрессирующим разрушением головного мозга, происходящим в результате гибели нервных клеток. Это заболевание получило название губчатой энцефалопатии. Похожие симптомы были известны давно, но наблюдались они не у человека, а у животных (скрейпи овец), и долгое время между ними не находили достаточной обоснованной связи.
Новый интерес к их изучению возник в 1996 г., когда в Великобритании появилась новая форма заболевания, обозначаемая как «новый вариант болезни Крейтцфельдта-Якоба (nvCJD)».
Важным событием было распространение «коровьего бешенства» в Великобритании, эпидемия которого была сначала в 1992—1993 гг, а потом и в 2001 г охватила несколько европейских государств, но тем не менее экспорт мяса во многие страны не был прекращён. Заболевание связывают с использованием «прионизированной» костной муки в кормах и премиксах, изготовленной из туш павших или заболевших животных, возможно, и не имевших явных признаков заболевания.
Пути переноса причинного фактора болезни, механизмы проникновения прионов в организм и патогенез заболевания изучены пока недостаточно.
В 1997 г. американскому врачу Стенли Прузинеру была присуждена Нобелевская премия за изучение прионов.
Свойства молекул
 |
В этом разделе не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена.Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники.Эта отметка установлена 12 мая 2011. |
|---|
Прионовые белки млекопитающих не сходны с прионовыми белками дрожжей по аминокислотной последовательности. Несмотря на это, основные структурные особенности (формирование амилоидных волокон и высокая специфичность, препятствующая передаче прионов от одного вида организмов к другому) у них общие. Вместе с тем, прион, отвечающий за коровье бешенство, обладает способностью передаваться от вида к виду.
Правый рисунок — модель двух конформаций приона; слева известная, нормальная, конформация структуры терминального участка C-terminal PrPC. (для отображения/загрузки см. RCSB Protein Databank).
Молекулярные основы патогенеза

Предполагаемый механизм «размножения» прионов.
В ходе исследований мозговых тканей умерших от прионных инфекций животных было показано, что прионы не содержат нуклеиновых кислот, а представляют собой белки.[1] Одним из первых охарактеризованных прионных белков стал PrP (от англ. prion-related protein или protease-resistant protein) массой около 35 кДа. Известно, что PrP может существовать в двух конформациях — «здоровой» — PrPC, которую он имеет в нормальных клетках (C — от англ. cellular — «клеточный»), в которой преобладают альфа-спирали, и «патологической» — PrPSc, собственно прионной (_Sc_- от scrapie), для которой характерно наличие большого количества бета-тяжей. При попадании в здоровую клетку, PrPSc катализирует переход клеточного PrPC в прионную конформацию. Накопление прионного белка сопровождается его агрегацией, образованием высокоупорядоченных фибрил (амилоидов), что в конце концов приводит к гибели клетки. Высвободившийся прион, по-видимому, оказывается способен проникать в соседние клетки, также вызывая их гибель.
Функции белка PrPC в здоровой клетке — поддержание качества миелиновой оболочки, которая в отсутствие этого белка постепенно истончается. В норме белок PrPC ассоциирован с клеточной мембраной, гликозилирован остатком сиаловой кислоты. Он может совершать циклические переходы внутрь клетки и обратно на поверхность в ходе эндо- и экзоцитоза[2]. Один такой цикл длится около часа.[источник не указан 908 дней] В эндоцитозном пузырьке или на поверхности клетки молекула PrPC может разрезаться протеазами на две примерно равные части[источник не указан 1309 дней].
До конца механизм спонтанного возникновения прионных инфекций не ясен. Считается (но ещё не полностью доказано), что прионы образуются в результате ошибок в биосинтезе белков. Мутации генов, кодирующих прионный белок (PrP), ошибки трансляции, процессы протеолиза — считаются главными кандидатами на механизм возникновения прионов. Согласно недавно проведённым исследованиям прионы способны к дарвиновской эволюции за счёт действия естественного отбора.[3]
Есть данные, дающие основание считать, что прионы являются не только инфекционными агентами, но и имеют функции в нормальных биопроцессах. Так, например, существует гипотеза, что через прионы осуществляется механизм генетически обусловленного стохастического старения.
Классификация
| Прионы млекопитающих — возбудители губчатой энцефалопатии | ||||
|---|---|---|---|---|
| ICTVdb Code | Заболевание | Носитель | Название приона | PrP изоформа |
| 90.001.0.01.001. | Скрейпи | овцы и козы | Прион скрейпи | OvPrPSc |
| 90.001.0.01.002. | Трансмиссивная энцефаломиопатия норок (ТЭН) | Норки | Прион ТЭН | MkPrPSc |
| 90.001.0.01.003. | Chronic wasting disease (CWD) | олени и лоси | CWD прион | MDePrPSc |
| 90.001.0.01.004. | Губчатая энцефалопатия крупного рогатого скота (ГЭКРС) | Коровы | Прион ГЭКРС | BovPrPSc |
| 90.001.0.01.005. | Губчатая энцефалопатия кошачьих (ГЭК) | Кошки | Прион ГЭК | FePrPSc |
| 90.001.0.01.006. | Губчатая энцефалопатия экзотических копытных (EUE) | Антилопы и большой куду | EUE прион | NyaPrPSc |
| 90.001.0.01.007. | Куру | Люди | Прион куру | HuPrPSc |
| 90.001.0.01.008. | Болезнь Крейцфельда-Якоба (БКЯ) | Люди | Прион БКЯ | HuPrPSc |
| (New) Variant Creutzfeldt-Jakob disease (vCJD, nvCJD) | Люди | vCJD прион | HuPrPSc | |
| 90.001.0.01.009. | Синдром Герстманна—Штройслера—Шейнкера (GSS) | Люди | GSS прион | HuPrPSc |
| 90.001.0.01.010. | Фатальная семейная бессонница (ФСБ) | Люди | Прион ФСБ | HuPrPSc |
Этиология
 |
В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена.Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники.Эта отметка установлена 12 мая 2011. |
|---|
Человек может заразиться прионами, содержащимися в пище, так как они не разрушаются ферментами пищеварительного тракта [источник не указан 1113 дней]. Так как стенками кишечника они не адсорбируются, то могут проникать в кровь только через поврежденные ткани. В конечном итоге они попадают в центральную нервную систему. Так переносится новый вариант болезни Крейтцфельдта-Якоба (nvCJD), которой люди заражаются после употребления в пищу говядины, содержащей нервную ткань из голов скота, больных бычьей губчатой энцефалопатией (BSE, коровье бешенство).
На практике доказана возможность прионов заражать организм мышей воздушно-капельным путем.
Прионы могут проникать в тело и парентеральным путем. Были описаны случаи заражения при внутримышечном введении препаратов, изготовленных из человеческих гипофизов (главным образом гормоны роста для лечения карликовости), а также заражение мозга инструментами при нейрохирургических операциях, поскольку прионы устойчивы к применяемым в настоящее время термическим и химическим методам стерилизации[источник не указан 984 дня]. Эта форма болезни Крейтцфельдта-Якоба обозначается как ятрогенная (1CJD).
При определённых, неизвестных условиях, в организме человека может произойти спонтанная трансформация прионного белка в прион. Так возникает так называемая спорадическая болезнь Крейтцфельдта-Якоба (sCJD), впервые описанная в 1920 г. независимо друг от друга Гансом Герхардом Крейтцфельдтом и Альфонсом Марией Якобом. Предполагается, что спонтанное возникновение этой болезни связано с фактом, что в норме в человеческом теле постоянно возникает небольшое количество прионов, которые эффективно ликвидируются клеточным Аппаратом Гольджи. Нарушение этой способности «самоочищения» клеток может привести к повышению уровня прионов выше допустимой границы нормы и к их дальнейшему неконтролируемому распространению. Причиной возникновения спорадической болезни Крейтцфельдта-Якоба согласно этой теории является нарушение функции Аппарата Гольджи в клетках[источник не указан 984 дня].
Особую группу прионовых заболеваний представляют собой наследственные (врожденные) болезни, вызванные мутацией гена прионового белка, который делает возникший прионовый белок более подверженным спонтанному изменению пространственной конфигурации и превращения их в прионы. К этой группе наследственных заболеваний относится и наследственная форма болезни Крейтцфельдта-Якоба (fCJD), которая наблюдается в ряде стран мира[источник не указан 984 дня].
При прионовой патологии наивысшая концентрация прионов обнаружена в нервной ткани заражённых людей. Прионы встречаются в лимфатической ткани. Наличие прионов в биологических жидкостях, включая слюну, пока не было однозначно подтверждено. Если представление о постоянном возникновении небольшого количества прионов верно, то можно предположить, что новые, более чувствительные методы диагностики откроют это количество прионов, разбросанное по различным тканям. В данном случае, однако, речь пойдёт о «физиологическом» уровне прионов, которые не представляют собой никакой угрозы для человека[источник не указан 984 дня].
Пути заражения
 |
В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена.Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники.Эта отметка установлена 12 мая 2011. |
|---|

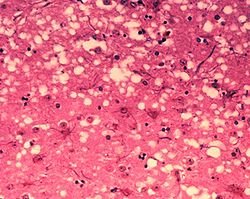
Гистологический препарат, поражение ткани прионами с образованием характерной губчатой структуры.
Очень мало известно о молекулярном характере прионов, вызывающих заболевания. Заражение могут вызвать примерно 100 000 молекул, которые в большинстве случаев образуют большие скопления. Значение агрегации отдельных молекул в ассоциации для вирулентности прионов — устойчивость к действию ферментов, расщепляющих белки, ставшие ненужными. Нельзя исключить, что вирулентными являются и отдельные молекулы прионов. Из некоторых экспериментов следует, что для возникновения прионов в ткани достаточно лишь временного контакта ткани с материалом, содержащим прионы, и нет необходимости, чтобы прионы были навсегда внесены в организм. Этот риск является актуальным, например, в связи с использованием хирургических инструментов, заражённых прионами. Процесс трансформации «здоровых» прионовых белков в прионы может быть инициирован простым контактом здоровых тканей с прионами, зафиксированными на хирургическом инструменте.
Ход болезни и распространение прионов по организму зависит от типа приона. Прионы отличаются составом аминокислот, характерных для данного вида, определяемых видовым геном прионового белка, а также так называемыми посттрансляционными модификациями или степенью гликозилирования базовой белковой цепочки. Посттрансляционная модификация значительно влияет на характеристики прионов и именно ей приписывают разницу между так называемыми прионовыми родами. В случае нового варианта (nvCJD) был пока что описан лишь один вид приона, сходный с прионами скота, заражённого бычьей губчатой энцефалопатией. Поэтому течение заболевания у человека и животных, заражённых новым вариантам, практически одинаково. У прочих видов живых существ, однако, известно много прионовых родов. У овец были описаны примерно два десятка таких родов, которые не вирулентны для человека. Течение овечьего прионового заболевания в зависимости от рода прионов значительно отличается — от очень быстрого, с практически внезапной гибелью, до медленного, затяжного.
Нетипичные случаи клинического течения нового варианта у скота, заражённого бычьей губчатой энцефалопатией, которые имели место в Японии и Италии[источник не указан 1113 дней], наводят на мысль о существовании большего количества родов бычьих прионов. Если бы этот род бычьих прионов попал в организм человека, следовало бы ожидать возникновение нового варианта с симптомами и клиническим течением, отличными от известных случаев.
У пациентов, больных болезнью Крейтцфельдта-Якоба, прионы распространяются в нервной системе, тканях глаза и лимфатических тканях, включая миндалины, селезенку, а также в слепой кишке. Наибольшее количество прионов находится в нервной системе, а наименьшее — в лимфатической ткани.
Пока что не был зарегистрирован ни один случай переноса нового варианта болезни Крейтцфельдта-Якоба (nvCJD) при медицинском вмешательстве, что является, разумеется, хорошей новостью. С другой стороны, специалисты предупреждают о преувеличенном оптимизме, прежде всего в условиях Великобритании, так как инкубационный период может быть достаточно долгим (от 5-8 месяцев до 10-15 лет).[источник не указан 1113 дней]
Прионы и медицинские инструменты
 |
В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена.Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники.Эта отметка установлена 12 мая 2011. |
|---|
Прионы очень стойки к обычным методам дезинфекции. Ионизирующее, ультрафиолетовое или микроволновое излучение на них практически не действует. Дезинфекционные средства, обычно используемые в медицинской практике, действуют на них лишь в очень ограниченной мере. Надёжно их ликвидируют дезинфицирующие реактивы — сильные окислители, разрушающе действующие на белки.[источник не указан 1113 дней]
Другое затруднение представляет собой стойкость прионов к высоким температурам. Даже при автоклавировании при 134 °C в течение 18 минут невозможно достичь полного разрушения прионов, и прионы «выживают» в форме, способной вызвать заражение. Стойкость к высоким температурам ещё более возрастает, если прионы засохнут на поверхности металла или стекла или если образцы перед автоклавированием были подвергнуты действию формальдегида.[источник не указан 1113 дней]
В Великобритании, где новый вариант является очень серьёзной проблемой, по этим причинам уже используются одноразовые хирургические инструменты для тонзиллэктомии. В будущем напрашивается альтернативное решение: создания новых инструментов, с учётом повышенных требований к очистке и обеззараживанию. Одноразовое использование инструментов согласно принципам ВОЗ требуется в случае стоматологического обслуживания пациентов с диагностированным прионным заболеванием или в случае подозрения на него.
Намного более сложным решением этой проблемы является лечение пациентов группы риска. К ним относятся пациенты, которые подверглись операциям, при которых была использована потенциально заражённая твёрдая мозговая оболочка, или пациенты из семей с наследственной формой болезни Крейтцфельдта-Якоба. ВОЗ в этом случае не требует никаких специальных мер. Британский Консультационный научный комитет по губчатой энцефалопатии в своём решении в 1998 г. счёл возможным ограничиться более тщательной очисткой и обеззараживанием инструментов, в сочетании с более длительным автоклавированием.
Прионные заболевания человека
Наиболее известные прионные инфекции человека, связанные с поражением головного мозга:
- болезнь Крейтцфельдта — Якоба (Creutzfeldt-Jakob disease), делится на iCJD, vCJD, fCJD, sCJD;
- фатальная семейная бессонница (Fatal Familial Insomnia);
- болезнь Куру (Kuru), связана с ритуальным каннибализмом народности Форе в восточной части Новой Гвинеи;
- синдром Герстманна — Штройслера — Шейнкера (Gerstmann-Sträussler-Scheinker disease).
Потенциальная опасность для человека
Несмотря на незначительное количество явных случаев прионных заболеваний у людей, многие специалисты считают, что имеется высокая степень опасности «медленных» инфекций для человека.
Имеются данные, что источником распространения могут быть стоматологические процедуры, связанные с попаданием прионов в кровяное русло.
Под подозрение попал также лецитин животного происхождения, что вызвало сокращение применения его в фармакологической промышленности, и вытеснение растительным (в основном, соевым) лецитином.
Исследования прионов дрожжей и других микромицетов


Известно, что в лабораторных и природных популяциях дрожжей и других микромицетов встречаются фенотипы, которые обусловлены не генетическими изменениями, а альтернативным состоянием одного из нормальных белков, которое обуславливает то или иное клеточное проявление. Исследования прионных фенотипов дрожжей подтвердили гипотезу о том, что эти проявления обусловлены только состоянием белка. Было показано, что прионы, экстрагированные из клеток, могут служить «семенами» образования прионов в пробирке. Один из наиболее хорошо изученных белков, склонных к образованию прионов у дрожжей — фактор терминации трансляции Sup35 (гомолог eRF3).
Клетки, в которых присутствует прионная форма Sup35, называются [PSI+] клетками. Такие клетки имеют изменённое физиологическое состояние и изменённый уровень выражения некоторых генов, что позволило выдвинуть гипотезу о том, что у дрожжей образование прионов может играть адаптативную роль[4]. Так, формирование прионов [PSI+] отменяет накопление красного пигмента, образующегося в результате мутации в гене ade1 (нижняя картинка), в результате чего колонии дрожжей становятся белыми (верхняя).
Кроме Sup35 известны также другие прионные белки Saccharomyces cerevisiae — Rnq1, Swi1, Ure3, Oct1, Cyc8.
Критика
Mark Purdy и David R. Brown предположили, что металлоионы, взаимодействуя с прионовыми белками, могут быть причиной развития прион-индуцированных (prion-mediated) заболеваний.[5]
Purdy провёл кластерное эпидемиологическое исследование при прионных заболеваниях в районах с низкой концентрацией меди в почвах.[источник не указан 1113 дней]
См. также
- Коровье бешенство
- Субвирусные частицы
- Список инфекционных заболеваний
Примечания
- ↑ http://www.antibiotic.ru/cmac/2000_2_2/012.htm прионы являются мелкими белковыми инфекционными частицами, устойчивыми к ферментативной инактивации
- ↑ Liberski PP, Brown DR, Sikorska B, Caughey B, Brown P. Cell death and autophagy in prion diseases (transmissible spongiform encephalopathies). Folia Neuropathol. 2008; 46(1):1-25.
- ↑ А.Марков. Дарвиновская эволюция без участия генов
- ↑ Galkin AP, Mironova LN, Zhuravleva GA, Inge-Vechtomov SG. (2006). «Yeast prions, mammalian amyloidoses, and the problem of proteomic networks». Genetica 42 (11): 1558. PMID 17163073.
- ↑ 2000-09-22, Normal Function of Prions, Statement to the BSE Inquiry
Литература
- И. С. Шкундина, М. Д. Тер-Аванесян. Прионы. Успехи биологической химии, т. 46, 2006 (обзор)
- Григорьев В. Б. — Прионные болезни человека и животных. — Вопросы вирусологии, т.49(№ 5), с.4-12, 2004 (обзор)
- Покровский В. И., Киселев О. И., Черкасский Б. Л. — Прионы и прионные болезни — РАМН, 2004, 384 стр., ISBN 5-7901-0038-4
- Prion biology and diseases, edited by S.B.Prusiner, Cold Spring Harbor, NY, 1999, ISBN 0-87969-547-1
Источники
- ing. Jaroslav Petr, DrSc. Phony a ustni dutina. Progresdent, 2004, № 2, s. 12-16
Ссылки
На английском языке
- Mad Cow Disease Информация о коровьем бешенстве, Center for Global Food Issues.
- Madcowering A BSE-TSE blog.
- The Pathological Protein — Mad Cow, Chronic Wasting, and Other Deadly Prion Diseases (2003, updated online 2005). Philip Yam, Scientific American magazine writer and News Editor.
- Прионные заболевания (2003). Dr. Sean Heaphy, Leicester University.
- Prion Diseases and the BSE Crisis (1997). Статья Stanley Prusiner — первооткрывателя прионов, из Science magazine.
- Britannica Nobel: Прион, 1997
- ICTVdb 90.001.0.01. Mammalian Prions
- Официальная страница сайта о болезни коровьего бешенства Mad Cow Disease
- News & Views on Mad Cow Disease, Mad Deer Disease, Chronic Wasting Disease, and Bovine Spongiform Encephalopathy
- Biography of Dr Prusiner
- Science Daily статья о вакцине против прионных заболеваний
- Science Daily article on transmission of prions through soil
- Хороший обзор по прионам из Science Creative Quarterly
На русском языке
- Прионы — новый класс возбудителей инфекционных заболеваний
- Патогенез и патологоанатомическая картина прионных болезней
 Субвирусные частицы Субвирусные частицы |
|
|---|---|
| Дефектная интерферированная РНК • Прионы • Сателлиты • Вирусоиды • Вироиды | |
| См. также | Вирусы-сателлиты |