Изохорный процесс | это... Что такое Изохорный процесс? (original) (raw)
| Тепловые процессы |
|---|
 |
| Статья является частью одноименной серии. |
| Адиабатический процесс |
| Изохорный процесс |
| Изобарный процесс |
| Изотермический процесс |
| Изоэнтропийный процесс |
| Изоэнтальпийный процесс |
| Политропный процесс |
| править |
| См. также «Физический портал» |
Изохорический или изохорный процесс (от др.-греч. ἴσος «равный» и χώρος «место») — термодинамический процесс, который происходит при постоянном объёме. Для осуществления изохорного процесса в газе или жидкости достаточно нагревать (охлаждать) вещество в сосуде, который не изменяет своего объёма.
При изохорическом процессе давление идеального газа прямо пропорционально его температуре (см. Закон Шарля). В реальных газах закон Шарля не выполняется.
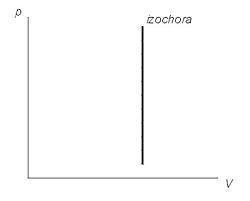
На графиках изображается линиями, которые называются изохоры. Для идеального газа они являются прямыми во всех диаграммах, которые связывают параметры: T (температура), V (объем) и P (давление).
Термодинамика процесса

График изохорного процесса на диаграмме (P,V)
Из определения работы следует, что изменение работы при изохорном процессе равно:

Чтобы определить полную работу процесса проинтегрируем данное выражение. Поскольку объем неизменен, то:
 ,
,
Но такой интеграл равен нулю. Итак, при изохорном процессе газ работы не совершает:
 .
.
Графически доказать это намного проще. С математической точки зрения, работа процесса — это площадь под графиком. Но график изохорного процесса является перпендикуляром к оси абсцисс. Таким образом, площадь под ним равна нулю.
Изменение внутренней энергии идеального газа можно найти по формуле:
 ,
,
где i — число степеней свободы, которое зависит от количества атомов в молекуле (3 для одноатомной (например, неон), 5 для двухатомной (например, кислород) и 6 для трёхатомной и более (например, молекула водяного пара)).
Из определения и формулы теплоёмкости и, формулу для внутренней энергии можно переписать в виде:
 ,
,
где  — молярная теплоёмкость при постоянном объёме.
— молярная теплоёмкость при постоянном объёме.
Используя первое начало термодинамики можно найти количество теплоты при изохорном процессе:

Но при изохорном процессе газ не выполняет работу. То есть, имеет место равенство:
 ,
,
то есть вся теплота, которую получает газ идёт на изменение его внутренней энергии.
Энтропия при изохорном процессе
Поскольку в системе при изохорном процессе происходит теплообмен с внешней средой, то происходит изменение энтропии. Из определения энтропии следует:

Выше была выведена формула для определения количества теплоты. Перепишем ее в дифференциальном виде:
 ,
,
где ν — количество вещества,  — молярная теплоемкостью при постоянном объеме. Итак, микроскопическое изменение энтропии при изохорном процессе можно определить по формуле:
— молярная теплоемкостью при постоянном объеме. Итак, микроскопическое изменение энтропии при изохорном процессе можно определить по формуле:

Или, если проинтегрировать последнее выражение, полное изменение энтропии в этом процессе:

В данном случае выносить выражение молярной теплоемкости при постоянном объеме за знак интеграла нельзя, поскольку она является функцией, которая зависит от температуры.
Список литературы
- Сивухин Д. В. Общий курс физики. — Издание 3-е, исправленное и дополненное. — М.: Наука, 1990. — Т. II. Термодинамика и молекулярная физика. — 592 с. — ISBN 5-02-014187-9
- Ландау, Л. Д., Лифшиц, Е. М. Статистическая физика. Часть 1. — Издание 5-е. — М.: Физматлит, 2005. — 616 с. — («Теоретическая физика», том V). — ISBN 5-9221-0054-8