Культура клеток | это... Что такое Культура клеток? (original) (raw)
Культивирование клеток представляет собой процесс, посредством которого in vitro отдельные клетки (или единственная клетка) прокариот и эукариот искусственно выращиваются в контролируемых условиях. На практике термин «культура клеток» относится в основном к выращиванию клеток, относящихся к одной ткани, полученных от многоклеточных эукариот, чаще всего животных. Историческое развитие технологии и методик выращивания культур клеток неразрывно связаны с выращиванием тканевых культур и целых органов.
Содержание
- 1 История
- 2 Основные принципы культивирования
- 3 Использование клеточных культур
- 4 Культуры клеток не млекопитающих
- 5 Виды клеточных линий
- 6 Краткий перечень клеточных линий
- 7 См. также
- 8 Ссылки и примечания
История
В XIX веке английский физиолог С. Рингер разработал солевой раствор[1], содержащий хлориды натрия, калия, кальция и магния для поддержания биения сердца животных вне организма. В 1885 году Вильгельм Ру установил принцип культивирования тканей, извлек часть костного мозга из куриного эмбриона и держал его в теплом физрастворе в течение нескольких дней[2]. Росс Гранвилл Харрисон, работавший в Медицинской школе Дж. Хопкинса, а затем в Йельском университете, опубликовал результаты своих экспериментов в 1907 −1910 годах, создав методологию культивирования тканей. В 1910 г. Пейтон Раус, работая с культурой клеток саркомы цыпленка, индуцировал образование опухолей у здоровых животных. Позже это привело к открытию онкогенных вирусов (Нобелевская премия по физиологии или медицине 1966 г.).
Методы культивирования клеток получили значительное развитие в 1940-х 1950-х годах в связи с исследованиями в области вирусологии. Выращивание вирусов в культурах клеток дало возможность получения чистого вирусного материала для производства вакцин. Вакцина против полиомиелита стала одним из первых препаратов, массово произведенных с использованием технологии культивирования клеток. В 1954 г. Эндерс, Уэллер и Роббинс получили Нобелевскую премию «За открытие способности вируса полиомиелита расти в культурах различных тканей». В 1952 г. была получена широко известная линия раковых клеток человека HeLa.
Основные принципы культивирования
Выделение клеток
Для культивирования вне организма живые клетки могут быть получены несколькими способами. Клетки могут быть выделены из крови, но к росту в культуре способны только лейкоциты. Моноядерные клетки могут быть выделены из мягких тканей с помощью таких ферментов как коллагеназа, трипсин, проназа, разрушающих внеклеточный матрикс[3]. Кроме того, в питательную среду можно поместить кусочки тканей.
Культуры клеток, взятых непосредственно от объекта (ex vivo), называются первичными[4]. Большинство первичных клеток, за исключением опухолевых, имеют ограниченный срок использования. После определенного количества делений клетки такие стареют и прекращают делиться, хотя могут при этом не утратить жизнеспособность.
Существуют иммортализованные («бессмертные») линии клеток, способные размножаться бесконечно. У большинства опухолевых клеток эта способность является результатом случайной мутации, но у некоторых лабораторных клеточных линий она приобретена искусственно, путем активации гена теломеразы[5].
Культивирование клеток
Клетки выращивают в специальных питательных средах, при постоянной температуре, а для клеток млекопитающих обычно необходима также специальная газовая среда, поддерживаемая в инкубаторе клеточных культур[6][7]. Как правило, регулируется концентрация в воздухе углекислого газа и паров воды, но иногда также и кислорода. Питательные среды для разных культур клеток различаются по составу, pH, концентрации глюкозы, составу факторов роста и др[8]. Факторы роста, используемые в питательных средах, чаще всего добавляют вместе с сывороткой крови. Одним из факторов риска при этом является возможность заражения культуры клеток прионами или вирусами. При культивировании одной из важных задач является исключение или сведение к минимуму использование зараженных ингредиентов. Однако на практике это бывает достигнуто не всегда. Наилучшим, но и наиболее дорогостоящим способом является добавление вместо сыворотки очищенных факторов роста[9].
Клетки можно выращивать в суспензии, либо в адгезивном состоянии. Некоторые клетки (такие, как клетки крови) в естественных условиях существуют во взвешенном состоянии. Существуют также линии клеток, искусственно измененных таким образом, чтобы они не могли прикрепляться к поверхности; это сделано для того, чтобы увеличить плотность клеток в культуре. Для выращивания адгезивных клеток требуется поверхность, например, культура ткани, или пластик, покрытый элементами внеклеточного матрикса для улучшения адгезивных свойств, а также для стимулирования роста и дифференцировки. Большинство клеток из мягких и твердых тканей адгезивны. Из адгезивного типа культуры выделяются органотипические культуры клеток, которые представляют собой трехмерную среду, в отличие от обычной лабораторной посуды. Этот система культивирования физически и биохимически наиболее сходна с живыми тканями, но имеет некоторые технические сложности в обслуживании (например, нуждается в диффузии).
Перекрестное загрязнение клеточных линий
При работе с клеточными культурами ученые могут столкнуться с проблемой перекрестного загрязнения.
Особенности выращивания клеток
При выращивании клеток, из-за постоянного деления может возникнуть их переизбыток в культуре. В результате чего могут возникнуть следующие проблемы:
- Накопление в питательной среде продуктов выделения, в том числе токсичных.
- Накопление в культуре омертвевших клеток, прекративших жизнедеятельность.
- Скопление большого количества клеток оказывает негативное влияние на клеточный цикл, рост и деление замедляются, а клетки начинают стареть и отмирать (контактное ингибирование роста).
- По той же причине может начаться клеточное дифференцирование.
Для поддержания нормального функционирования культур клеток а также для предотвращения негативных явлений периодически проводят замену питательной среды, пассажирование и трансфекция клеток. Во избежание загрязнения культур бактериями, дрожжами, или другими линиями клеток, все манипуляции обычно проводят с соблюдением правил асептики в стерильном боксе. Для подавления микрофлоры в питательную среду могут быть добавлены антибиотики (пенициллин, стрептомицин) и противогрибковые препараты(амфотерицин Б).
Одним из продуктов метаболизма в клетках являются кислоты, вследствие чего pH среды постепенно снижается. Для контроля кислотности питательных сред, в них добавляют индикаторы pH. Если культура клеток адгезивная, питательную среду можно полностью заменять.
Пассажирование клеток
Пассажирование (разделение) клеток — это отбор небольшого количества клеток для выращивания в другом лабораторном сосуде. Если культура быстро растет, это необходимо делать регулярно, поскольку в среде истощаются питательные вещества и накапливаются продукты метаболизма. Суспензивные культуры пассажировать проще, так как для этого достаточно всего лишь отобрать необходимое количество клеток, поместить их в другие сосуды, и добавить свежей питательной среды. Адгезивные же клетки перед этим следует отделить от субстрата и разделить их скопления. Чаще всего для этой цели используют смесь трипсина и ЭДТА или другие ферментные смеси, иногда достаточно только ЭДТА в физиологическом растворе (раствор Версена). Если культура растет медленно, ее обычно подкармливают без переноса в другой сосуд, периодически (обычно раз в 2-3 дня) отбирая часть использованной среды и добавляя свежую.
Трансфекция и трансдукция
В клетки при их выращивании можно внедрять чужеродную ДНК путем трансфекции (невирусный метод). Часто данную технологию применяют для управляемой экспрессии генов. Сравнительно недавно для этих целей была успешно реализована трансфекция иРНК.
ДНК также может быть внедрена в геном клетки с помощью вирусов или бактериофагов. Они, являясь внутриклеточными паразитами, как нельзя лучше подходят для этих целей, так как внедрение генетического материала в клетку-хозяина является обычной частью их жизненного цикла[10]. Этот метод называется трансдукция.
Линии клеток человека

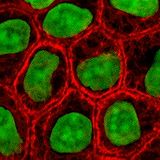
Одна из самых ранних культур клеток человека, полученная от Генриетты Лакс, которая умерла от рака шейки матки. Культура клеток HeLa окрашена по Хойсту. Измененные ядра окрашены в синий цвет.
Культивирование человеческих клеток несколько противоречит правилам биоэтики, поскольку изолированно выращиваемые клетки могут пережить родительский организм, а затем использоваться для проведения экспериментов или для разработки новых методов лечения и извлечения из этого прибыли. Первое судебное решение в данной области было вынесено в Верховном суде штата Калифорния по делу «Джон Мур против представителей Калифорнийского университета», согласно которому пациенты не имеют никаких прав собственности на линии клеток, полученных из органов, удаленных с их согласия[11].
Гибридома
Гибридома — это линия клеток, полученнаая в результате слияния нормальных лимфоцитов с «бессмертными» раковыми клетками. Используется для получения моноклональных антител. Лейкоциты, выделенные из селезенки или крови иммунизированных животных, производят антитела с необходимой специфичностью, но как у любой первичной культуры, их способность к пролиферации ограничена лимитом Хейфлика. Для иммортализации их искусственно сливают с «бессмертной» линией клеток миеломы, в результате чего происходит рекомбинация признаков. После этого линию клонируют и отбирают клоны, способные одновременно к неограниченной пролиферации и производящие антитела против избранного антигена.
Использование клеточных культур
Массовое культивирование клеток является основой для промышленного производства вирусных вакцин и разнообразных продуктов биотехнологии.
Продукты биотехнологии
Промышленным методом из культур клеток получают такие продукты, как ферменты, синтетические гормоны, моноклональные антитела, интерлейкины, лимфокины, противоопухолевые препараты. Хотя многие простые белки относительно просто могут быть получены с использованием рДНК в бактериальных культурах, более сложные белки, такие как гликопротеины, в настоящее время могут быть получены только из животных клеток. Одним из таких важнейших белков является гормон эритропоэтин. Стоимость выращивания культур клеток млекопитающих является довольно высокой, поэтому в настоящее время проводятся исследования по возможности производства сложных белков в культурах клеток насекомых или высших растений.
Тканевые культуры
Культивирование клеток является неотъемлемой частью технологии культивирования тканей и тканевой инженерии, поскольку именно оно определяет основы выращивания клеток и поддержания их в жизнеспособном состоянии ex vivo.
Вакцины
С применением методики культивирования клеток в настоящее время выпускаются вакцины против полиомиелита, кори, эпидемического паротита, краснухи, ветрянки. Вследствие угрозы пандемии гриппа, вызываемого штаммом вируса H5N1, в настоящий момент правительство Соединенных Штатов финансирует исследования по получению вакцины против птичьего гриппа с использованием клеточных культур.
Культуры клеток не млекопитающих
Культуры клеток растений
Культуры клеток растений, как правило, выращиваются либо в виде суспензии в жидкой питательной среде, либо в виде каллусной культуры на твердой питательной основе. Культивирование недифференцированных клеток и каллуса требует соблюдения определенного баланса гормонов роста растений ауксинов и цитокининов.
Бактериальные, дрожжевые культуры
Основная статья: Бактериальная культура
Для культивирования небольшого количества клеток бактерий и дрожжей клетки высеивают на твердую питательную среду на основе желатина или агар-агара. Для массового производства применяют выращивание в жидких питательных средах (бульонах).
Вирусные культуры
Культуры вирусов выращивают на культурах клеток млекопитающих, растений, грибов или бактерий, в зависимости от природного хозяина конкретного типа вирусов. Но при некоторых условиях могут быть выращены и в клетках другого типа.
В этом случае культура клеток сама служит средой для роста и репликации вируса.
Виды клеточных линий
Краткий перечень клеточных линий
Приведенный здесь список наиболее распространенных клеточных линий не является полным и исчерпывающим.
| Линия клеток | Расшифровка сокращения | Организм | Ткань | Морфология | Примечания и ссылки |
|---|---|---|---|---|---|
| 293-T | человек | почка(эмбриональная) | Производная от HEK-293 ECACC | ||
| 3T3 cells | "3-day transfer, inoculum 3 x 105 cells" | мышь | эмбриональные фибробласты | Известна также как NIH 3T3 ECACC | |
| 721 | человек | меланома | |||
| 9L | крыса | глиобластома | |||
| A2780 | человек | яичник | рак яичника | ECACC | |
| A2780ADR | человек | яичник | производное A2780 с резистентностью к адриамицину | ECACC | |
| A2780cis | человек | яичник | производное A2780 с резистентностью к цисплатину | ECACC | |
| A172 | человек | глиобластома | злокачественная глиома | ECACC | |
| A431 | человек | кожный эпителий | плоскоклеточная карцинома | ECACCCell Line Data Base | |
| A-549 | человек | карцинома легких | эпителий | DSMZECACC | |
| B35 | крыса | нейробластома | ATCC | ||
| BCP-1 | человек | периферические лейкоциты | HIV+ лимфома | ATCC | |
| BEAS-2B | bronchial epithelium + adenovirus 12-SV40 virus hybrid (Ad12SV40) | человек | легкие | эпителий | ATCC |
| bEnd.3 | brain endothelial | мышь | кора головного мозга | эндотелий | ATCC |
| BHK-21 | "Baby Hamster Kidney" | хомяк | почка | фибробласты | ECACCOlympus |
| BR 293 | человек | молочная железа | рак | ||
| BxPC3 | Biopsy xenograph of pancreatic carcinoma line 3 | человек | панкреатическая аденокарцинома | эпителий | ATCC |
| C3H-10T1/2 | мышь | эмбриональные мезенхимальные клетки | ECACC | ||
| C6/36 | Кусака бело-пёстрый (комар) | ткани личинки | ECACC | ||
| CHO | Chinese hamster ovary | серый хомячок (Cricetulus griseus) | яичник | эпителий | ECACCICLC |
| COR-L23 | человек | легкие | ECACC | ||
| COR-L23/CPR | человек | легкие | ECACC | ||
| COR-L23/5010 | человек | легкие | ECACC | ||
| COR-L23/R23 | человек | легкие | эпителий | ECACC | |
| COS-7 | Cercopithecus aethiops, origin-defective SV-40 | обезьяна Cercopithecus aethiops | почка | фибробласты | ECACCATCC |
| CML T1 | Chronic Myelod Leukaemia T-lymphocyte 1 | человек | хроническая миелоидная лейкемия | T-клеточная лейкемия | Blood |
| CMT | canine mammary tumor | собака | молочная железа | эпителий | |
| D17 | собака | остеосаркома | ECACC | ||
| DH82 | собака | гистиоцитоз | моноциты/макрофаги | ECACC J Vir Meth | |
| DU145 | человек | карцинома | простата | ||
| DuCaP | Dura mater Cancer of the Prostate | человек | метастазирующий рак простаты | эпителий | 11317521 |
| EL4 | мышь | T-клеточная лейкемия | ECACC | ||
| EMT6/AR1 | мышь | молочная железа | эпителий | ECACC | |
| EMT6/AR10.0 | мышь | молочная железа | эпителий | ECACC | |
| FM3 | человек | метастазы в лимфатический узел | меланома | ||
| H1299 | человек | легкие | рак | ||
| H69 | человек | легкие | ECACC | ||
| HB54 | гибридома | гибридома | секретирует L243 mAb (против HLA-DR) | Human Immunology | |
| HB55 | гибридома | гибридома | секретирует MA2.1 mAb (против HLA-A2 и HLA-B17) | Journal of Immunology | |
| HCA2 | человек | фибробласты | Journal of General Virology | ||
| HEK-293 | human embryonic kidney | человек | почка(эмбриональная) | эпителий | ATCC |
| HeLa | Henrietta Lacks | человек | рак шейки матки | эпителий | DSMZECACC |
| Hepa1c1c7 | clone 7 of clone 1 hepatoma line 1 | мышь | гепатома | эпителий | ECACC ATCC |
| HL-60 | human leukemia | человек | миелобласты | клетки крови | ECACCDSMZ |
| HMEC | human mammary epithelial cell | человек | эпителий | ECACC | |
| HT-29 | человек | эпителий толстого кишечника | аденокарцинома | ECACC Cell Line Data Base | |
| Jurkat | человек | T-клеточная лейкемия | белые клетки крови | ECACC DSMZ | |
| JY | человек | лимфобласты | В-клетки, иммортализованные EBV | ||
| K562 | человек | лимфобласты | хроническая миелоидная лейкемия | ECACC | |
| Ku812 | человек | лимфобласты | эритролейкемия | ECACC LGCstandards | |
| KCL22 | человек | лимфобласты | хроническая миелоидная лейкемия | ||
| KYO1 | Kyoto 1 | человек | лимфобласты | хроническая миелоидная лейкемия | DSMZ |
| LNCap | Lymph node Cancer of the Prostate | человек | аденокарцинома простаты | эпителий | ECACCATCC |
| Ma-Mel 1, 2, 3....48 | человек | линии клеток меланомы | |||
| MC-38 | мышь | аденокарцинома | |||
| MCF-7 | Michigan Cancer Foundation-7 | человек | молочная железа | инвазивная карцинома протоков молочной железы | ER+, PR+ |
| MCF-10A | Michigan Cancer Foundation | человек | молочная железа | эпителий | ATCC |
| MDA-MB-231 | M.D. Anderson - Metastatic Breast | человек | молочная железа | рак | ECACC |
| MDA-MB-468 | M.D. Anderson - Metastatic Breast | человек | молочная железа | рак | ECACC |
| MDA-MB-435 | M.D. Anderson - Metastatic Breast | человек | молочная железа | меланома или карцинома (единого мнения нет) | Cambridge Pathology ECACC |
| MDCK II | Madin Darby canine kidney | собака | почка | эпителий | ECACC ATCC |
| MOR/0.2R | человек | легкие | ECACC | ||
| NCI-H69/CPR | человек | легкие | ECACC | ||
| NCI-H69/LX10 | человек | легкие | ECACC | ||
| NCI-H69/LX20 | человек | легкие | ECACC | ||
| NCI-H69/LX4 | человек | легкие | ECACC | ||
| NIH-3T3 | National Institutes of Health, 3-day transfer, inoculum 3 x 105 cells | мышь | эмбрион | фибробласты | ECACCATCC |
| NALM-1 | периферическая кровь | хроническая миелоидная лейкемия | Cancer Genetics and Cytogenetics | ||
| NW-145 | меланома | ESTDAB | |||
| OPCN / OPCT | Onyvax[1] Prostate Cancer.... | линии клеток рака простаты | Asterand | ||
| Peer | человек | T-клеточная лейкемия | DSMZ | ||
| PNT-1A / PNT 2 | линии клеток рака простаты | ECACC | |||
| RenCa | Renal Carcinoma | мышь | карцинома почки | ||
| RIN-5F | мышь | поджелудочная железа | |||
| RMA/RMAS | мышь | T-клеточный рак | |||
| Saos-2 | человек | остеоксаркома | ECACC | ||
| Sf-9 | Spodoptera frugiperda | бабочка Spodoptera frugiperda | яичник | DSMZECACC | |
| SkBr3 | человек | карцинома молочной железы | |||
| T2 | человек | гибридома В-клеток и Т-клеточной лейкемии | DSMZ | ||
| T-47D | человек | молочная железа | карцинома протоков | ||
| T84 | человек | карцинома толстого кишечника/ метастазы в легкое | эпителий | ECACCATCC | |
| THP1 | человек | моноциты | острая миелоидная лейкемия | ECACC | |
| U373 | человек | глиобластома-астроцитома | эпителий | ||
| U87 | человек | глиобластома-астроцитома | эпителий | Abcam | |
| U937 | человек | лейкемическая моноцитарная лимфома | ECACC | ||
| VCaP | Vertebra Prostate Cancer | человек | метастазирующий рак простаты | эпителий | ECACC ATCC |
| Vero | 'Vera Reno' ('почка зеленой') / 'Vero' ('истина') | африканская зеленая мартышка | эпителий почки | ECACC | |
| WM39 | человек | кожа | первичная меланома | ||
| WT-49 | человек | лимфобласты | |||
| X63 | мышь | меланома | |||
| YAC-1 | мышь | лимфома | Cell Line Data Base ECACC | ||
| YAR | человек | B-лимфоциты | трансформированы EBV | [2] Human Immunology |
См. также
- Биологическое бессмертие
- Культура тканей
- Выращивание органов
- Биотехнология
- Индуцированные стволовые клетки
- Ниша стволовой клетки
Ссылки и примечания
- ↑ Раствор Рингера
- ↑ http://caat.jhsph.edu/pubs/animal_alts/appendix_c.htm
- ↑ Клетки можно выделить из тканей и разделить на различные типы
- ↑ ЛабоRUтория Культивирование клеток и тканей. www.primer.ru (2003).(недоступная ссылка — история) Проверено 27 марта 2010.
- ↑ Теломераза. Тёмная материя (15 сентября 2006). Архивировано из первоисточника 28 марта 2012. Проверено 27 марта 2010.
- ↑ Инкубаторы СО2 Binder (Германия). Техсервис. Архивировано из первоисточника 8 июня 2012. Проверено 27 марта 2010.
- ↑ Лабораторное оборудование и расходные материалы. Инкубаторы (2007). Архивировано из первоисточника 8 июня 2012. Проверено 27 марта 2010.
- ↑ С помощью сред определенного химического состава можно идентифицировать специфические факторы роста
- ↑ LipiMAX purified lipoprotein solution from bovine serum. Selborne Biological Services (2006). Архивировано из первоисточника 8 июня 2012. Проверено 27 марта 2010.
- ↑ Механизм инфицирования вируса
- ↑ В.Богомолова Кому принадлежит наше тело?. Arcanus (3 августа 2009). Архивировано из первоисточника 8 июня 2012. Проверено 27 марта 2010.