Олигопептиды | это... Что такое Олигопептиды? (original) (raw)
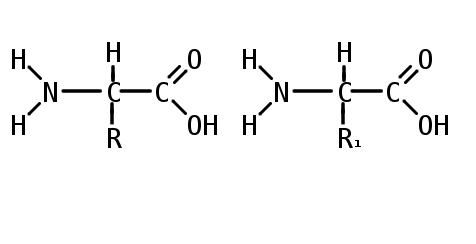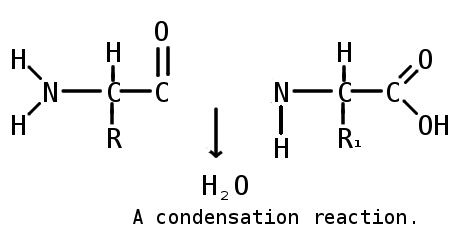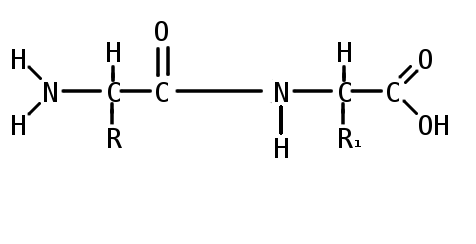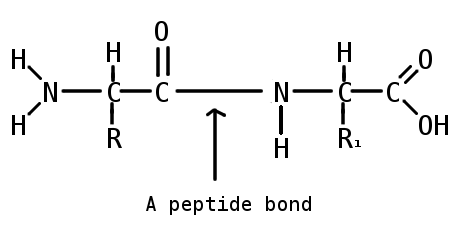
Образование пептидной связи

Пример пептидной молекулы — гормон окситоцин.
Пептиды (греч. πεπτος — питательный) — семейство веществ, молекулы которых построены из остатков α-аминокислот, соединённых в цепь пептидными (амидными) связями —C(O)NH—.
Это природные или синтетические соединения, содержащие десятки, сотни или тысячи мономерных звеньев — аминокислот. Полипептиды состоят из сотен аминокислот, в противоположность олигопептидам, состоящим из небольшого числа аминокислот (не более 10-50), и простым пептидам (до 10).
- Полипептиды могут иметь в молекуле неаминокислотные фрагменты, например углеводные остатки.
- Природные полипептиды с молекулярной массой более 6000 дальтон называют белками.
Содержание
- 1 Терминология: Олигопептиды и Полипептиды
- 2 История
- 3 Известные «семейства» пептидов
- 4 Терминология по теме
- 5 См. также
- 6 Внешние ссылки
Терминология: Олигопептиды и Полипептиды
Грань между олигопептидами и полипептидами (тот размер, при котором белковая молекула перестаёт считаться олигопептидом и становится полипептидом) достаточно условна. Часто пептиды, содержащие менее 10-20 аминокислотных остатков, называют олигопептидами, а вещества с большим числом аминокислотных звеньев — полипептидами. Во многих случаях эта грань в научной литературе не проводится вообще и небольшая белковая молекула (такая, как окситоцин) упоминается как полипептид (или просто как пептид).
История
Пептиды впервые были выделены из гидролизатов белков, полученных с помощью ферментирования.
- Термин пептид предложен Э. Фишером, который к 1905 г. разработал общий метод синтеза пептидов.
В 1953 В. Дю Виньо синтезировал окситоцин, первый полипептидный гормон. В 1963 г., на основе концепции твердофазного пептидного синтеза (P. Меррифилд) были созданы автоматические синтезаторы пептидов. Использование методов синтеза полипептидов позволило получить синтетический инсулин и др. ферменты.
Известные «семейства» пептидов
Семейства пептидов в этом разделе являются рибосомальными, обычно они обладают гормональной активностью.
Панкреатические молекулы полипептидного характера
- en:NPY
- Пептид YY
- APP Avian pancreatic polypeptide
- en:HPP Human pancreatic polypeptide
Опиоидные пептиды
Опиоидные пептиды — группа природных и синтетических пептидов, сходных с опиатами (морфин, кодеин и др.) по способности связываться с опиоидными рецепторами организма. Эндогенные морфиноподобные вещества были впервые выделены в 1975 году из целого мозга и гипофиза голубей, морских свинок, крыс, кроликов и мышей, а в 1976 году фракции таких олигопептидов были обнаружены в спинномозговой жидкости и крови человека . Различные виды этих олигопептидов получили название эндорфинов и энкефалинов. Лиганды опиоидных рецепторов были обнаружены и во многих периферических органах, тканях и биологических жидкостях. Присутствие опиоидов показано в гипоталамусе и гипофизе, плазме крови и спиномозговой жидкости, желудочно-кишечном тракте, лёгких, органах репродуктивной системы, иммунокомпетентных тканях и даже в коже. Наряду с эндорфинами обнаружены и так называемые экзорфины или параопиоиды — опиоидные пептиды, образующиеся при переваривании пищи. К настоящему времени опиоидные рецепторы и их эндогенные лиганды обнаружены практически во всех органах и тканях млекопитающих, а также у животных более низких ступеней классификации вплоть до простейших. Основная часть опиоидных пептидов образуется путём внутриклеточного расщепления высокомолекулярных предшественников, что приводит к образованию ряда биологически активных фрагментов, в том числе и опиоидных пептидов. Идентифицированы и наиболее изучены 3 таких предшественника: проопиомеланокортин (ПОМК), проэнкефалин А и продинорфин (проэнкефалин В). В состав ПОМК (локализованного главным образом в гипофизе) входят аминокислотные последовательности b-липотропина, АКТГ, a-, b- и g-меланоцитстимулирующих гормонов, a-, b- и g-эндорфинов. В настоящее время установлено, что основным источником энкефалинов (метионин-энкефалина и лейцин-энкефалина) в организме является проэнкефалин А, локализованный преимущественно в надпочечниках. В его составе содержится 4 аминокислотные последовательности мет-энкефалина и одна лей-энкефалина, а также ряд продленных форм мет-энкефалина: меторфамид, МЕРГЛ (мет-энкефалин-Arg6-Gly7-Leu8), МЕРФ (мет-энкефалин-Arg6-Phe7), пептид Ф и группы родственных пептидов, входящих в состав пептида Е: BAM 22, 20, 18, 12, взаимодействующих с опиоидными рецепторами mu-, kappa- и delta-типа. В структуре другого проэнкефалина — препроэнкефалина В (или продинорфина) — обнаружены последовательности a- и b-неоэндорфинов, динорфинов [динорфин 1-8, 1-17 (А), динорфин В (риморфин), 4кД-динорфин], обладающих наибольшим сродством к ОР k-типа, а также лей-энкефалина. Радиорецепторный анализ связывания эндорфинов и энкефалинов с опиоидными рецепторами показал, что сродство мет- и лей-энкефалинов к опиоидным рецепторам delta-типа выше, чем к рецепторам mu-типа; b-эндорфин имеет примерно одинаковое сродство к опиоидным рецепторам mu- и delta-типа, a- и g-эндорфины проявляют гораздо меньшее сродство к обоим типам рецепторов по сравнению с b-эндорфином. Несмотря на то, что мет-энкефалин взаимодействует преимущественно с опиоидными рецепторами d-типа, его аналоги с более длинной аминокислотной последовательностью — меторфамид и пептиды группы BAM (пептиды из мозгового вещества надпочечников) обладают противоположным профилем селективности взаимодействия с опиоидными рецепторами (mu > kappa > delta). Большинство эндогенных опиоидов в той или иной степени могут взаимодействовать с несколькими типами рецепторов. Так, b-эндорфин своим N-концевым фрагментом способен взаимодействовать с mu- и delta-опиоидными рецепторами, а С-концом с epsilon-рецепторами. В коже амфибий, а затем и в мозге и некоторых других органах теплокровных, обнаружен 4-ый предшественник ОП — продерморфин, который считается источником дерморфина (mu-агониста) и дельторфина (delta-агониста). В ЦНС обнаружены эндогенные пептиды, специфически взаимодействующие с mu-опиоидными рецепторами: Tyr-Pro-Trp-Phe-NH2 и Tyr-Pro-Phe-Phe-NH2, названные эндоморфинами, а также пептид ноцицептин, оказывающий свой анальгетический эффект через опиоидоподобные орфановые рецепторы.
Пептиды (Tachykinin peptides)
- Субстанция Р
- en:Kassinin
- Нейрокинин А (en:Neurokinin A)
- en:Eledoisin
- Нейрокинин В (en:Neurokinin B)
Терминология по теме
- Полипептиды простая линейная цепь, состоящая из аминокислот
- Олигопептиды или (просто) пептиды — полипептиды с числом аминокислот в цепи до 30-50
- Дипептиды
- Трипептиды
- Гексапептиды
- Нейропептиды пептиды, ассоциированные с нервной тканью
- Пептидные гормоны — петиды с Гормональной активностью
См. также
Внешние ссылки
| Органические вещества | |
|---|---|
| Углеводороды | Алканы · Алкены · Алкины · Диены · Циклоалканы · Арены |
| Кислородсодержащие | Спирты · Простые эфиры · Альдегиды · Кетоны · Кетены · Карбоновые кислоты · Сложные эфиры · Углеводы · Жиры · Хиноны |
| Азотсодержащие | Амины · Амиды · Нитросоединения · Нитрозосоединения · Оксимы · Нитрилы · Аминокислоты · Белки · Пептиды |
| Серосодержащие | Меркаптаны · Тиоэфиры · Сульфокислоты · Тиоальдегиды · Тиокетоны · Тиокарбоновые кислоты |
| Фосфорсодержащие | Фосфины · Фосфонистые кислоты · Фосфиновые кислоты · Фосфоновые кислоты · Нуклеиновые кислоты · Нуклеотиды |
| Кремнийорганические | Силаны · Силазаны · Силтианы · Силоксаны · Силиконы |
| Элементоорганические | Германийорганические · Борорганические · Оловоорганические · Свинецорганические · Алюминийорганические · Ртутьорганические · Другие металлоорганические |
| Другие важные классы | Галогенуглеводороды · Гетероциклические соединения · Перфторуглеводороды |
Wikimedia Foundation.2010.