Щавелевая кислота | это... Что такое Щавелевая кислота? (original) (raw)
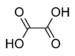
| Щавелевая кислота | |
|---|---|
 |
|
| Номенклатура | |
| Тривиальное название | щавелевая кислота |
| Систематическое название | этандиовая кислота |
| Брутто-формула | H2C2O4 |
| Свойства | |
| Молярная масса | 90,04 г/моль |
| Внешний вид | бесцветные моноклинныекристаллы |
| Плотность | 1,36 г/см³ |
| Растворимость в воде (г на 100г) | 10 (20 °C); 25 (44,5 °C); 120 (100 °C) |
| Растворимость в этаноле, ацетоне, диэтиловом эфире | хорошо растворима |
| Температура плавления | 189,5 °C |
| Температура возгонки | 125 °C |
| Температура разложения | 100-130 °C |
| Температура кипения(при 100 мм.рт.ст.) | - |
| Температурадекарбоксилирования | 166-180 °C |
| Константы кислотности | K1 5,6·10−2; K2 6,4·10−5 |
| Динамическая вязкость (η) | - |
| Абсолютная величина дипольного момента (μ) | 0,1·10−30 Кл·м |
| Теплоёмкость (C0p) | 108,8 Дж/(моль·град) |
| Энтальпия образования (Δ_H0_обр) | −817,38 кДж/моль |
| Энтальпия возгонки (Δ_H0_возг) | 90,58 кДж/моль |
| Энтальпия сгорания (Δ_H0_сгор) | −251,8 кДж/моль |
| Энтальпия растворения (Δ_H0_раств) | −9,58 кДж/моль |
| Энтальпия плавления (Δ_H0_пл) | - |
| Энтальпия испарения (Δ_H0_исп) | - |
Щаве́левая кислота (этандиовая кислота) НООССООН — двухосновная предельная карбоновая кислота. Принадлежит к сильным органическим кислотам. Обладает всеми химическими свойствами, характерными для карбоновых кислот. Соли и эфиры щавелевой кислоты называются оксалатами. В природе содержится в щавеле, ревене, карамболе и некоторых других растениях в свободном виде и в виде оксалатов калия и кальция. Впервые щавелевая кислота синтезирована в 1824 году немецким химиком Фридрихом Вёлером из дициана. Щавелевая кислота (или оксалат-ион C2O42−) является восстановителем (обесцвечивает раствор KMnO4).
В промышленности щавелевую кислоту получают окислением углеводов, спиртов и гликолей смесью HNO3 и H2SO4 в присутствии V2O5, либо окислением этилена и ацетилена HNO3 в присутствии PdCl2 или Pd(NO3)2, а также окислением пропилена жидким NO2. Перспективен способ получения щавелевой кислоты из CO через формиат натрия:
Свойства некоторых производных щавелевой кислоты:
| Соединение | Молярная масса | tпл, °C | tкип | _d_204 | _n_20D |
|---|---|---|---|---|---|
| Диметилоксалат(COOCH3)2 | 118,088 | 54 | 163,5 | 1,148(54 °C) | - |
| Диэтилоксалат(COOC2H5)2 | 146,14 | −40,6 | 185,4 | 1,0785 | 1,4104 |
| Дибутилоксалат(COOC4H9)2 | 202,24 | −29,6 | 245,5 | 0,9873 | 1,424 |
| Оксалилхлорид(COCl)2 | 126,93 | −12 | 64 | 1,43 | 1,434 (12,9 °C) |
| Оксамид(CONH2)2 | 88,072 | 419 | - | - | - |
| Циан (дициан)(CN)2 | 52,035 | −27,83 | −21,3 | 0,9577(-26,89 °C) | - |
Применение
В лабораториях щавелевую кислоту иногда применяют для получения хлороводорода и иодоводорода:

Также щавелевая кислота используется для лабораторного синтеза диоксида хлора:

Щавелевую кислоту и оксалаты находят применение в текстильной и кожевенной промышленности как протрава. Они служат компонентами анодных ванн для осаждения металлических покрытий — алюминия, титана и олова покрытий. Щавелевая кислота и оксалаты являются реагентами, используемыми в аналитической и органической химии. Он входят в составы для удаления ржавчины и оксидных плёнок на металле; применяются для осаждения редкоземельных элементов.
Производные щавелевой кислоты — диалкилоксалаты, главным образом диэтилоксалат и дибутилоксалат — применяются как растворители целлюлозы. Ряд сложных эфиров щавелевой кислоты и замещённых фенолов используются как хемилюминесцентные реагенты.
Опасность
Щавелевая кислота и её соли токсичны, ПДК в воде водоёмов хозяйств бытового пользования — 0,2 мг/л.
Литература
- Зефиров Н.С. и др. т.5 Три-Ятр // Химическая энциклопедия. — М.: Большая Российская Энциклопедия, 1998. — 783 с. — ISBN 5-85270-310-9