Диоксид-дихлорид хрома | это... Что такое Диоксид-дихлорид хрома? (original) (raw)
| Диоксид-дихлорид хрома | |
|---|---|
 |
|
 |
|
| Общие | |
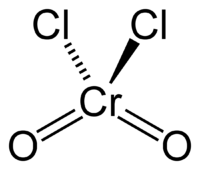
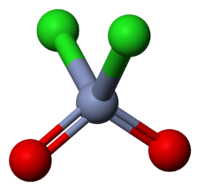
| Систематическое наименование | Диоксид-дихлорид хрома(VI) |
| Химическая формула | CrO2Cl2 |
| Физические свойства | |
| Состояние (ст. усл.) | кроваво-красная дымящеяся жидкость |
| Молярная масса | 154.9008 г/моль |
| Плотность | 1.911 г/см³ |
| Термические свойства | |
| Температура плавления | -96.5 °C |
| Температура кипения | 117 °C |
| Химические свойства | |
| Растворимость в воде | растворяется г/100 мл |
| Структура | |
| Кристаллическая структура | тетраэдральная |
| Классификация | |
| Рег. номер CAS | 14977-61-8 |
| SMILES | Cl[Cr](Cl)(=O)=O |
| RTECS | GB5775000 |
| Безопасность | |
| Токсичность |    |
Диоксид-дихлорид хрома (хлористый хромил) — это жидкость тёмно-красного цвета, дымится во влажном воздухе.
Содержание
Свойства
Химические
Диоксид-дихлорид хрома является молекулярным соединением. Это означает, что в жидких и твердых агрегатных состояниях молекулы данного соединения будут взаимодействовать исключительно с помощью сил Ван-дер-Ваальса. Такая слабая связь приводит к низким температурам плавления и кипения. CrO2Cl2 является очень электрофильным веществом и агрессивным окислителем; самовозгорается при капании на аморфную серу. При гидролизе в продуктах реакции получаются хромовая и соляная кислоты:

Его высокая реакционная способность по отношению к воде указывает на тот факт, что CrO2Cl2 способен дымиться во влажном воздухе.
Получение
Диоксид-дихлорид хрома получается при воздействии хлороводорода на оксид хрома(VI) (формула CrO3) или реакции с К2СrО4 с концентрированной соляной кислотой, а затем с добавлением серной кислоты в качестве обезвоживающего агента. CrO2Cl2 отделяется в виде густой жидкости. Затем он может быть отделен с помощью простой дистилляции. CrO2Cl2 также может быть получен добавлением концентрированной серной кислоты в смесь хлорида натрия и бихромата калия, а затем с последующей отгонкой продукта.

Опасность применения
Дихлорид-диоксида хрома является очень агрессивным реагентом. Активно реагирует с водой, спиртами и другими сильно электрофильными веществами, такими как хлористый водород и соединения шестивалентного хрома (CrVI). CrVI может приводить к хромосомным аберрациям. Частые воздействия на кожу веществом могут привести к её изъязвлениям. Хлористый водород может привести к поражению органов дыхания, вплоть до летального исхода. Воздействие паров диоксида-дихлорида хрома может привести к раздражению дыхательных путей, сильному раздражению глаз и ожогам кожи и глаз. При попадании внутрь может вызвать серьёзные отравления и повреждения внутренних органов.
Литература
- Реми Г. т.II // Курс неорганической химии. — М.: Мир, 1966. — 836 с.
| Соединения хрома |
|---|
| Бихромат аммония ((NH4)2Cr2O7) • Борид хрома (CrB) • Бромид хрома(II) (CrBr2) • Бромид хрома(III) (CrBr3) • Гексагидроксохромат (III) натрия (Na3[Сr(OH)6]) • Гексакарбонил хрома (Cr(CO)6) • Гидроксид хрома (III) (Cr(OH)3) • Гидроксид хрома(II) (Cr(OH)2) • Двухромовая кислота (H2Cr2O7) • Диоксид-дихлорид хрома (CrO2Cl2) • Дихромат калия (K2Cr2O7) • Дихромат лития (Li2Cr2O7) • Дихромат натрия (Na2Cr2O7) • Дихромат рубидия (Rb2Cr2O7) • Дихромат цезия (Cs2Cr2O7) • Зелень Гинье (Cr2O3•nH2O) • Иодид хрома(II) (CrI2) • Иодид хрома(III) (CrI3) • Карбид хрома(II) (Cr3C2) • Нитрат хрома (Cr(NO3)3) • Нитрид хрома (CrN) • Оксид хрома(II) (CrO) • Оксид хрома(III) (Cr2O3) • Оксид хрома(IV) (CrO2) • Оксид хрома(VI) (CrO3) • Оксифторид хрома(III) (CrOF) • Ортофосфат хрома(III) (CrPO4) • Пероксид хрома(VI) (CrO5) • Сульфат хрома(II) (CrSO4) • Сульфат хрома(III) (Cr2(SO4)3) • Сульфид хрома(II) (CrS) • Сульфид хрома(III) (Cr2S3) • Сульфат хрома(III)-калия (KCr(SO4)2) Фосфат хрома (CrPO4) • Фосфид хрома (CrP) • Фторид хрома(II) (CrF2) • Фторид хрома(III) (CrF3) • Фторид хрома(IV) (CrF4) • Фторид хрома(V) (CrF5) • Фтористый хромил (CrO2F2) • Хлорид гексаамминхрома(III) ([Сr(NH3)6]Cl3) • Хлорид хрома(II) (CrCl2) • Хлорид хрома(III) (CrCl3) • Хлорид хрома(IV) (CrCl4) • Хлористый хромил (CrO2Cl2) • Хромат аммония ((NH4)2CrO4) • Хромат калия (K2CrO4) • Хромат лития (Li2CrO4) • Хромат натрия (Na2CrO4) • Хромат рубидия (Rb2CrO4) • Хромат серебра (Ag2CrO4) • Хромат цезия (Cs2CrO4) • Хромит железа(II) (Fe(CrO2)2) • Хромит калия (KCrO2) • Хромовая кислота (H2CrO4) • |