Метилглиоксаль | это... Что такое Метилглиоксаль? (original) (raw)
| Метилглиоксаль | |
|---|---|
 |
|
 |
|
| Общие | |
| Систематическое наименование | 2-оксопропаналь |
| Химическая формула | C3H4O2 |
| Физические свойства | |
| Состояние (ст. усл.) | жидкость |
| Молярная масса | 72.0627 г/моль |
| Плотность | 1,0455 г/см³ |
| Термические свойства | |
| Температура кипения | 72 °C |
| Классификация | |
| Рег. номер CAS | 78-98-8 |
| SMILES | CC(=O)C=O |
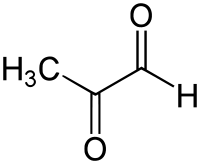
Метилглиоксаль (пирувальдегид, 2-оксопропаналь) — альдегид пировиноградной кислоты, является одновременно альдегидом и кетоном.
Биология
В живых организмах метилглиоксаль образуется как побочный продукт нескольких метаболических путей. [1] Он может образоваться из 3-аминоацетона, промежуточного продукта катаболизма треонина либо в процессе перекисного окисления липидов. Однако, важнейший источник метилглиоксаля — гликолиз, где он получается в процессе неферментативного гидролиза фосфатной группы от глицеральдегид-фосфата и дигидроацетон-фосфата, двух промежуточных компонентов гликолиза. Метилглиоксаль является цитотоксическим продуктом, поэтому в клетке существует несколько механизмов инактивации, в том числе глиоксалазная система. Метилглиоксаль реагирует в клетке с глутатионом, образуя гемитиоацеталь, который превращается в _S_-D-лактоилглутатион под действием глиоксалазы I [2] и далее метаболизируется в D-лактат под действием глиоксалазы II. [3]
Патология
В силу своей реактивности метилглиоксаль играет большую роль в образовании поздних продуктов гликирования в процессе реакции Майяра. Более того, он считается важнейшим из гликирующих реагентов (т. е. ковалентно связывающихся с амино-группами белков, таких как глюкоза, галактоза и др.), приводящих к нарушению функций белков при диабете. [4].
См. также
Ссылки
- ↑ Inoue Y, Kimura A (1995). «Methylglyoxal and regulation of its metabolism in microorganisms». Adv. Microb. Physiol. 37: 177–227. PMID 8540421.
- ↑ Thornalley PJ (2003). «Glyoxalase I--structure, function and a critical role in the enzymatic defence against glycation». Biochem. Soc. Trans. 31 (Pt 6): 1343–8. DOI:10.1016/S0006-2952(99)00132-X. PMID 14641060.
- ↑ Vander Jagt DL (1993). «Glyoxalase II: molecular characteristics, kinetics and mechanism». Biochem. Soc. Trans. 21 (2): 522–7. PMID 8359524.
- ↑ Shinohara M (1998). «Overexpression of glyoxalase-I in bovine endothelial cells inhibits intracellular advanced glycation endproduct formation and prevents hyperglycemia-induced increases in macromolecular endocytosis.». J Clin Invest. 101 (5): 1142–7. DOI:10.1172/JCI119885. PMID 9486985.