Таутомерия | это... Что такое Таутомерия? (original) (raw)

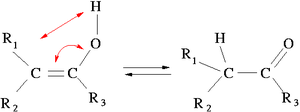
Обратимый переход из енол- в кето- форму
Таутомери́я (от греч. ταύτίς — тот же самый и μέρος — мера) — явление обратимой изомерии, при которой два или более изомера легко переходят друг в друга. При этом устанавливается таутомерное равновесие, и вещество одновременно содержит молекулы всех изомеров (таутомеров) в определённом соотношении.
Чаще всего при таутомеризации происходит перемещение атомов водорода от одного атома в молекуле к другому и обратно в одном и том же соединении. Классическим примером является ацетоуксусный эфир, представлющий собой равновесную смесь этилового эфира ацетоуксусной (I) и оксикротоновой кислот (II).
Таутомерия сильно проявляется для целого круга веществ, производных циановодорода. Так уже сама синильная кислота существует в двух таутомерных формах:

При комнатной температуре равновесие превращения циановодорода в изоциановодород смещено влево. Показано, что менее стабильный изоциановодород более токсичен.

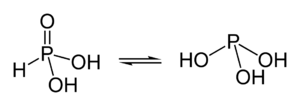
Таутомерные формы фосфористой кислоты
Аналогичное превращение известно для циановой кислоты, которая известна в трёх изомерных формах, однако таутомерное равновесие связывает только две из них: циановую и изоциановую кислоты:

Для обеих таутомерных форм известны сложные эфиры, т. е. продукты замещения в циановой кислоте водорода на углеводородные радикалы. В отличие от указанных таутомеров третий изомер – гремучая (фульминовая) кислота не способна к самопроизвольному превращению в другие формы.
С явлением таутомерии связаны многие химико-технологические процессы, особенно в области синтеза лекарственных веществ и красителей (производство витамина С — аскорбиновой кислоты в др.). Очень важна роль таутомерии в процессах, протекающих в живых организмах.
Амид-иминольную таутомерию лактамов называют лактам-лактимной таутомерией. Она играет большую роль в химии гетероциклических соединений. Равновесие в большинстве случаев смещено в сторону лактамной формы.