Фторид хлора(I) | это... Что такое Фторид хлора(I)? (original) (raw)
| Фторид хлора(I) | |
|---|---|
 |
|
 |
|
| Общие | |
| Систематическое наименование | Фторид хлора (I) |
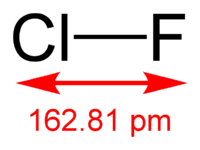
| Химическая формула | ClF |
| Физические свойства | |
| Состояние (ст. усл.) | бледно-жёлтый газ |
| Отн. молек. масса | 54 а. е. м. |
| Молярная масса | 54,45 г/моль |
| Плотность | (жидкость, −100 °C) 1,62 г/см³ |
| Термические свойства | |
| Температура плавления | −155,6 °C |
| Температура кипения | −100,1 °C |
| Классификация | |
| Рег. номер CAS | 7790-89-8 |
Фторид хлора(I) (монофторид хлора, фтористый хлор) — ClF, соединение хлора с фтором, представляющее собой при комнатной температуре бесцветный ядовитый тяжёлый газ с сильным разражающим запахом. Конденсируется при охлаждении до −100 °C в жидкость бледно-жёлтого цвета. Многие свойства сходны со свойствами фтора и хлора.
Содержание
- 1 Физико-химические свойства
- 2 Методы получения
- 3 Химические свойства
- 4 Применение
- 5 Литература
- 6 Примечания
- 7 См. также
Физико-химические свойства
| Свойство | Значение |
|---|---|
| Диэлектрическая проницаемость | 0,881 |
| Энтальпия образования (298К, в газовой фазе) | −56,5 кДж/моль |
| Энтропия образования (298К, в газовой фазе) | 217,91 Дж/(моль·К) |
| Энтальпия парообразования | 20,16 кДж/моль |
| Теплоёмкость (298К, в газовой фазе) | 32,22 Дж/(моль·К) |
В ИК-спектрах наблюдается полоса поглощения 747 см−1 (для твёрдого вещества).
Методы получения
- Одним из методов получения фторида хлора является метод, предложенный Доманжем и Хейдорфером[1]. В этом методе через аппарат, состоящий из медных трубок, пропускают смесь хлора и фтора в соотношении 1:1 при 220—230°С:
Cl2 + F2 → 2ClF
- ClF также получают из трифторида хлора и хлора. Так как в настоящее время трифторид хлора производится в промышленном масштабе, то этот метод получил большое распространение:
ClF3 + Cl2 → 3 ClF
Химические свойства
Химически очень активное вещество; по своей активности в некоторых реакциях превосходит фтор. Хороший фторирующий агент. За счет того, что атом хлора находится в степени окисления +1, проявляет сильные окислительные свойства.
4ClF + 2H2O → 2Cl2 + O2 + 4HF
- При нагревании очень активно реагирует с водородом. При этом образуются фтороводород и хлороводород:
ClF + H2 → HCl + HF
- Реагирует с хлоридами металлов с образованием фторидов и хлора:
NaCl + ClF → NaF + Cl2
- При взаимодействии с простыми веществами образуются фториды:
Br2 + 6ClF → 2BrF3 + 3Cl2
Si + 4ClF → 2SiF4 + 2Cl2
W + 6ClF → WF6 + 3Cl2
- С монооксидом углерода проходит реакция хлорфторирования:
CO + ClF → COClF
CsF + ClF → CsClF2
- Необычное полимерное соединение фиолетового цвета состава (F3ClO2)n было получено при взаимодействии ClF и O2F2:
nClF + nO2F2 → (F3ClO2)n
Применение
- Применяется как фторирующий агент в органическом синтезе,[2] а также как хлорирующий агент[3][4].
- Также достаточно перспективно использование монофторида хлора для отчистки фторидов урана[5]:
4ClF + UO2F2 → O2 + 2Cl2 + UF6
Литература
- Химия галоидных соединений фтора. Николаев Н. С., Сухоруков В. Ф., Шишков Ю. Д., Аленчикова И. Ф. — М.: Наука, 1968, с.-344.
Примечания
- ↑ L. Domange, S. Heudorffer Compt. rend. 1948, V. 226., P. 920.
- ↑ Богуславская Л. С. Фториды галогенов в органическом синтезе — Успехи химии, 1984, Том 53, C.2024-2055.
- ↑ Symmetry of chloronium ions from ionic reaction of chlorine, chlorine monofluoride gas, and chlorine monofluoride complex with terminal alkenes Shellhamer, Peter, Heasley. Journal of Fluorine Chemistry V. 124, P. 17-20
- ↑ The reactions of chlorine monofluoride with unsaturated compounds and the dehydrohalogenation of some of the derivatives G. Gambaretto, M.Napoli Journal of Fluorine Chemistry V. 7, P. 569—580
- ↑ Chemistry of the chlorine trifluoride-uranyl fluoride reaction R. Shrewsberry, L. Williamson Journal of Inorganic and Nuclear Chemistry V. 28, 1966, P. 2535—2539
См. также
| Соединения фтора |
|---|
| Гексафторалюминат натрия (Na3AlF6) • Гексафтороантимонат водорода (HSbF6) • Гексафторид платины (PtF6) • Гексафторид селена (SeF6) • Гексафторид теллура (TeF6) • Гексафторогерманат калия (K2[GeF6]) • Гексафторогерманат рубидия (Rb2[GeF6]) • Гексафторогерманат цезия (Cs2[GeF6]) • Гексафторосиликат(IV) калия (K2[SiF6]) • Гексафторосиликат натрия (Na2SiF6) • Гексафторплатинат ксенона (XePtF6) • Гексафторсиликат аммония ((NH4)2SiF6) • Гептафторид рения (ReF7) • Гептафторониобат(V) калия (K2[NbF7]) • Гидрофторид аммония ([NH4][HF2]) • Гидрофторид калия (HF2K) • Декафторид дисеры (S2F10) • Диоксидифторид (F2O2) • Диоксидифторид молибдена(VI) (MoF2O2) • Дифтордиазин (N2F2) • Дифторид радона (F2Rn) • Кремнефтористоводородная кислота (H2SiF6) • Монофторид алюминия (AlF) • Монофторид углерода (CF) • Оксид-фторид урана (UO2F2) • Окситетрафторид вольфрама(VI) (WOF4) • Окситетрафторид молибдена(VI) (MoOF4) • Оксифторид иттрия (YOF) • Оксифторид лантана(III) (LaOF) • Оксотетрафторид ксенона (XeOF4) • Оксотрифторид ванадия(V) (F3OV) • Пентафторид висмута (BiF5) • Пентафторид мышьяка (AsF5) • Пентафторид сурьмы (SbF5) • Пентафторид урана (UF5) • Пентафторид фосфора (PF5) • Субфторид серебра (Ag2F) • Тетрафторалюминат калия (KAlF4) • Тетрафтороборат лития (LiBF4) • Тетрафтороборат меди(II) (Cu(BF4)2) • Тетрафтороборат натрия (NaBF4) • Тетрафтороборат нитрозила (BF4NO) • Тетрафтороборат нитрония (BNO2F4) • Тетрафтороборат серебра (AgBF4) • Тетрафторборная кислота (HBF4) • Тетрафторид дибора (B2F4) • Тетрафторид кремния (SiF4) • Тетрафторид селена (SeF4) • Тетрафторид теллура (TeF4) • Тетрафторгидразин (N2F4) • Трифторид алюминия (AlF3) • Трифторид бора (BF3) • Трифторид мышьяка (AsF3) • Трифторид висмута (BiF3) • Трифторид сурьмы (SbF3) • Трифторид тиазила (NSF3) • Трифторид фосфора (PF3) • Фторфосфат натрия (Na2PFO3) • Фторамин (NH2F) • Фторид азота(III) (NF3) • Фторид аммония (NH4F) • Фторид бария (BaF2) • Фторид бериллия (BeF2) • Фторид брома(I) (BrF) • Фторид брома(III) (BrF3) • Фторид брома(V) (BrF5) • Фторид ванадия(III) (VF3) • Фторид ванадия(IV) (VF4) • Фторид ванадия(V) (VF5) • Фторид вольфрама(VI) (WF6) • Фторид галлия(III) (GaF3) • Фторид гафния(IV) (HfF4) • Фторид дейтерия (DF) • Фторид диртути(2+) (Hg2F2) • Фторид железа(II) (FeF2) • Фторид железа(III) (FeF3) • Фторид золота(III) (AuF3) • Фторид золота(V) (AuF5) • Фторид индия(III) (InF3) • Фторид иода(I) (IF) • Фторид иода(III) (IF3) • Фторид иода(V) (IF5) • Фторид иода(VII) (IF7) • Фторид иридия(IV) (IrF4) • Фторид иридия(V) (IrF5) • Фторид иридия(VI) (IrF6) • Фторид иттербия(III) (YbF3) • Фторид иттрия (YF3) • Фторид иттрия-лития (LiYF4) • Фторид кадмия (CdF2) • Фторид калия (KF) • Фторид кальция (CaF2) • Фторид кислорода(II) (OF2) • Фторид кобальта(II) (CoF2) • Фторид кобальта(III) (CoF3) • Фторид криптона(II) (KrF2) • Фторид ксенона(II) (XeF2) • Фторид ксенона(IV) (XeF4) • Фторид ксенона(VI) (XeF6) • Фторид лития (LiF) • Фторид магния (MgF2) • Фторид марганца(II) (MnF2) • Фторид марганца(III) (MnF3) • Фторид меди(I) (CuF) • Фторид меди(II) (CuF2) • Фторид молибдена(VI) (MoF6) • Фторид натрия (NaF) • Фторид никеля(II) (NiF2) • Фторид ниобия(V) (NbF5) • Фторид нитрозила) (NOF) • Фторид оксида азота(IV) (NO2F) • Фторид оксида серы(IV) (SO2F2) • Фторид олова(II) (SnF2) • Фторид олова(IV) (SnF4) • Фторид плутония(III) (PuF3) • Фторид плутония(IV) (PuF4) • Фторид плутония(VI) (PuF6) • Фторид радия (RaF2) • Фторид рения(IV) (ReF4) • Фторид рения(VI) (ReF6) • Фторид рения(VII) (ReF7) • Фторид ртути(II) (HgF2) • Фторид рубидия (RbF) • Фторид самария(III) (SmF3) • Фторид свинца(II) (PbF2) • Фторид серебра(I) (AgF) • Фторид серебра(II) (AgF2) • Фторид серы(IV) (SF4) • Фторид серы(VI) (SF6) • Фторид скандия(III) (ScF3) • Фторид стронция (SrF2) • Фторид таллия(I) (TlF) • Фторид тантала(V) (TaF5) • Фторид теллура(IV) (TeF4) • Фторид технеция(VI) (TcF6) • Фторид тиазила (NSF) • Фторид тианила (SOF2) • Фторид титана(III) (TiF3) • Фторид титана(IV) (TiF4) • Фторид тория(IV) (ThF4) • Фторид урана(III) (UF3) • Фторид урана(IV) (UF4) • Фторид урана(V) (UF5) • Фторид урана(VI) (UF6) • Фторид хлора(I) (ClF) • Фторид хлора(III) (ClF3) • Фторид хлора(V) (ClF5) • Фторид хрома(III) (CrF3) • Фторид хрома(IV) (CrF4) • Фторид хрома(V) (CrF5) • Фторид цезия (CsF) • Фторид цинка (ZnF2) • Фторид циркония(IV) (ZrF4) • Фторид-хлорид оксида серы(IV) (ClFO2S) • Фторноватистая кислота (HOF) • Фтороводород (HF) • Фторосульфоновая кислота (FSO3H) • Фторид хлорила (ClO2F) • Фторид перхлорила (ClO3F) • Фторид оксиперхлорила (ClO3OF) |