Диоксолан | это... Что такое Диоксолан? (original) (raw)
| Диоксолан | |
|---|---|
 |
|
 |
|
| Общие | |
| Систематическое наименование | 1,3-диоксолан |
| Химическая формула | C3H6O2 |
| Физические свойства | |
| Молярная масса | 74.08 г/моль |
| Плотность | 1.06 г/см³ |
| Термические свойства | |
| Температура плавления | -95 °C |
| Температура кипения | 75 °C |
| Классификация | |
| Рег. номер CAS | 646-06-0 |
| SMILES | O1COCC1 |
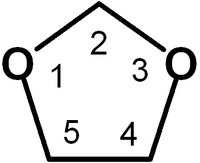
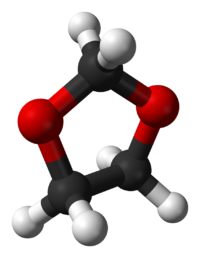
Диоксолан — органическое соединение класса пятичленных гетероциклов, в котором имеется два мостиковых атома кислорода. В зависимости от положения атомов кислорода различают 1,2- и 1,3-диоксолан.

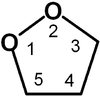
1,2-диоксолан

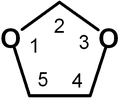
1,3-диоксолан
Содержание
1,2-диоксолан
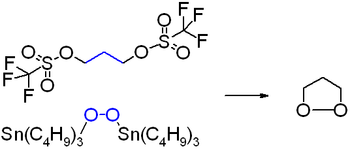
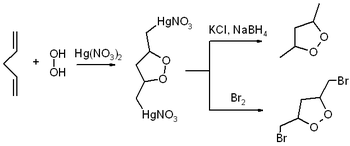
1,2-диоксоланы является циклическими пероксидами, и поэтому нестабильны: сам 1,2-диоксолан устойчив только до 35 °C. Его производные легко разлагаются при нагревании и облучении[1]. Получают по следующим схемам.


Соединения содержащие структуру 1,2-диоксолана, — промежуточные продукты в биосинтезе эндо-пероксидов простагландинов.
1,3-диоксолан
Химические свойства

2-бромэтилформиат
1,3-диоксолан легко растворяется в воде, с иодом образует комплекс, с бромом реагирует, образуя 2-бромэтилформиат. С хлором реакция приводит к смеси замещенных по 2-ом или 4-ом положении.
Применение
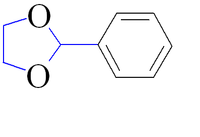
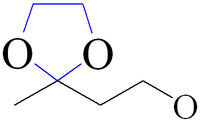
- 1,3-диоксолан можно рассматривать как циклический ацеталь формальдегида и этиленгликоля, а замещенные по второму положению 1,3-диоксоланы - как ацетали других альдегидов или кетонов.
Перевод в 1,3-диоксоланы является защитой для альдегидов и кетонов[2] или 1,2-диолов[3], поскольку они устойчивы к действию оснований и устойчивы в нейтральной среде.

Защита альдегидной группы

Защита кетогруппы

Защита 1,2-диолов
- Используется в качестве как экстрагента для жиров, масел, восков.
- В качестве низкокипящего растворителя красок и эфиров целлюлозы.
- При перемешивании раствора реагентов в присутствии ортоэфиров как водопоглощающего средства[4].
Методы синтеза
- 1,3-диоксолан получают из формалина и этиленгликоля кипячением в присутствии фосфорной кислоты[5].
- 2-замещённые 1,3-диоксоланы кипячением смеси альдегида и этиленгликоля в бензоле (толуоле, хлороформе, ксилоле, трихлорэтилене, дихлорметане) в присутствии пара-толуолсульфокислоты с азеотропной отгонкой образующейся воды и катализе пара-толуолсульфокислотой.
- обменным способом, когда кетон смешивается с диоксоланом более летучего кетона (ацетон, 2-бутанон и др.). При кипячении в присутствии пара-толуолсульфокислоты происходит обмен и более летучий кетон покидает сферу реакции, смещая равновесие в нужную сторону.
- реакцией этиленоксида с кетонами или альдегидами в присутствии SnCl4
Примечания
- ↑ Химическая энциклопедия Т2. — М.: Сов. Энциклопедия, 1990. — С. 74.
- ↑ Дж. МакОми. Защитные группы в органической химии. — М.: Мир, 1976. — С. 305–307.
- ↑ W. Theilheimer. Synthetic Methods of Organic Chemistry. Interscience Publ. Inc., V 13, 1959, p. 34.
- ↑ TETRAHEDRON, 1983, 39, N 6, 991–997.
- ↑ И. Губен. Методы органической химии, том 3 выпуск 1. — М.-Л.: ОНТИ, 1934.
- ↑ J. AMER. CHEM. SOC., 1982, 104, N 3, 853–855.
- ↑ J. CHEM. RES. SYNOP., 1980, NO 18, 95 (M 1163–1173)
 Кислородсодержащие гетероциклы Кислородсодержащие гетероциклы |
|
|---|---|
| Трёхчленные | Оксиран · Диоксиран |
| Четырёхчленные | Оксетан · Оксетанон (β-лактон) |
| Пятичленные | Фуран · Дигидрофуран · Тетрагидрофуран · Бензофуран · Изобензофуран · Диоксолан · Тетрагидрофуранон (γ-лактон) |
| Шестичленные | Пиран · Дигидропиран · Тетрагидропиран · Диоксан · Тетрагидропиранон (δ-лактон) |
| Семичленные | Капролактон (ε-лактон) |