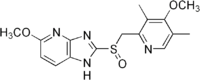Ингибиторы протонного насоса | это... Что такое Ингибиторы протонного насоса? (original) (raw)
Ингиби́торы прото́нного насо́са (синонимы: Ингиби́торы прото́нной по́мпы, Ингиби́торы прото́нового насо́са, Ингиби́торы прото́новой по́мпы; часто употребляется аббревиатура ИПП, реже — ИПН) — лекарственные препараты, предназначенные для лечения кислотозависимых заболеваний желудочно-кишечного тракта за счёт снижения продукции соляной кислоты посредством блокирования в париетальных клетках слизистой оболочки желудка протонного насоса — Н+/К+-АТФазы. Относятся к антисекреторным препаратам.

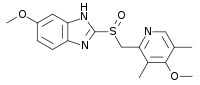
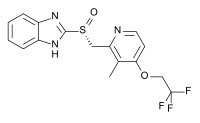
Омепразол — исторически первый ингибитор протонного насоса

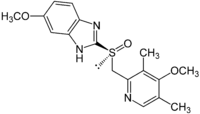
Тенатопразол
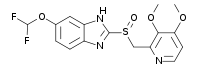
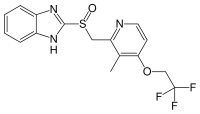
По химическому строению все ингибиторы протонного насоса являются производными бензимидазола и имеют единое молекулярное ядро. Различаются ингибиторы протонного насоса только химическими радикалами, которые придают им индивидуальные свойства, касающиеся длительности латентного периода, продолжительности времени действия препарата, особенностей рН-селективности, взаимодействия с другими одновременно принимаемыми препаратами и т. п.
Содержание
- 1 Из истории ингибиторов протонного насоса
- 2 Клиническое использование
- 3 Механизм действия
- 4 Фармакокинетика
- 5 Место ингибиторов протонного насоса среди других противоязвенных препаратов
- 6 Критерии оценки антисекреторного эффекта препаратов
- 7 Влияние генетических особенностей на терапию ИПП
- 8 Омепразоловая резистентность
- 9 Ночной кислотный прорыв
- 10 Подбор индивидуальной терапии антисекреторными препаратами
- 11 Общие характеристики ингибиторов протонного насоса
- 12 Противопоказания и ограничения при применении ИПН
- 13 Ингибиторы протонного насоса в классификаторах и перечнях
- 14 Примечания
- 15 Источники
- 16 Ссылки
- 17 См. также
Из истории ингибиторов протонного насоса
Первый опытный образец ИПП был синтезирован в 1974 году, в 1975 г. появился первый промышленный образец — тимопразол. Первый препарат из группы ИПП — омепразол был синтезирован в 1979 году[1] в Швеции в «Хэссле» — дочерней фирме компании «АстраЗенека» группой исследователей под руководством Ивана Эстхольма[2]. Он был представлен под торговым наименованием «Лосек» в 1988 году в Риме на Всемирном конгрессе гастроэнтерологов[3]. Этот конгресс признал ингибиторы протонного насоса основной группой кислотоконтролирующих лекарственных средств[1].
«Лосек» имел очень большой коммерческий успех (даже больший, чем появившийся в 2001 году более совершенный «Нексиум» (эзомепразол) той же фирмы). В 1991 году специалисты крупнейшей японской фармацевтической фирмы «Такеда» синтезировали ИПП лансопразол, который стал одним из её самых успешных продуктов[4].
Успехи в создании антисекреторных препаратов привели к тому, что уменьшилось число операций язвенных больных, в частности, операций ваготомии и, в 1993 году, на конференции гастроэнтерологов в Йеле, было принято соглашение о том, что операция ваготомии не может рассматриваться как метод выбора в лечении язвенной болезни[3].
Клиническое использование
Ингибиторы протонного насоса применяются при лечении широко круга заболеваний желудочно-кишечного тракта, в том числе:
- диспепсии[5],
- синдрома Золлингера — Эллисона[6],
- язвенной болезни желудка и двенадцатиперстной кишки[7][8],
- гастроэзофагеальной рефлюксной болезни[9],
- хронического гастрита и дуоденита[10][11],
- пищевода Барретта[12],
- ларингофагеальной рефлюксной болезни и респираторных рефлюкс-индуцированных заболеваний[13], в том числе, рефлюкс-индуцированной бронхиальной астмы[14],
- хронического панкреатита[15],
- ишемической болезни сердца, отягощённой ГЭРБ[16].
Современный подход к терапии кислотозависимых заболеваний часто предполагает отказ от терапии одним типом препарата, и заключается в том, что лечение производится комплексом препаратов по определённой, международно признанной «схеме»[17].
Механизм действия
За продукцию кислоты в желудке отвечают париетальные клетки фундальных желёз. Центральным звеном в секреции соляной кислоты является водородно-калиевая аденозинтрифосфатаза (Н+/К+-АТФаза), которая, будучи встроенная в апикальную (направленную в просвет желудка) мембрану париетальной клетки, выполняет роль протонного насоса, обеспечивающего перенос ионов водорода Н+ через мембрану в пространство желудка в обмен на ионы калия К+ в направлениях, противоположных электрохимическому градиенту для обоих ионов, используя для этого энергию гидролиза молекулы аденозинтрифосфорной кислоты (АТФ). После чего ион калия К+ уже по электрохимическому градиенту транспортируется обратно, вызывая совместный с ним перенос в просвет желудка иона хлора Cl−.
Молекулы ингибиторов протонного насоса, накапливаясь во внутриклеточных канальцах париетальных клеток в непосредственной близости от молекул Н+/К+-АТФазы, после некоторых преобразований трансформируются в тетрациклический сульфенамид, который ковалентно включается в цистеиновые группы Н+/К+-АТФазы, делая, тем самым, последнюю неспособной участвовать в процессе транспортировки ионов.
Фармакокинетика
Место ингибиторов протонного насоса среди других противоязвенных препаратов
В соответствии с современными представлениям о причинах язвенной болезни и других кислотозависимых заболеваний, важнейшим фактором их развития является нарушение равновесия между кислотно-пептической агрессией и защитными механизмами слизистой оболочки. Препараты, используемые для лечения этих заболеваний, действуют преимущественно либо на звено агрессии, уменьшая объём соляной кислоты и пепсина, либо на защитное звено, стимулируя защитные свойства слизистой оболочки. К последним относят цитопротекторы, препараты, имеющие различные механизмы действия, направленные на стабилизацию защитных свойства слизистой оболочки, заживление эрозий и язв, восстановление структуры и функции эпителия желудочно-кишечного тракта[18].
Антациды уменьшают кислотность желудочного содержимого за счет химического взаимодействия с соляной кислотой. Однако, на попытку нейтрализации кислоты щёлочью организм отвечает увеличением кислотопродукции. Таким образом, кислотность желудочного сока не только не снижается, а часто даже повышается, особенно после окончания действия препарата. Возникает так называемый «кислотный рикошет». Поэтому современные антацидные препараты, кроме кислотонейтрализации, выполняют функции по стимуляции секреции гидрокарбонатов, увеличивают синтез гликопротеинов желудочной слизи, предохраняют эпителий капилляров от ульцерогенных факторов, связывают лизолецитин и жёлчные кислоты[19].
Антихолинергические средства (М-холиноблокаторы) ингибируют М-холинорецепторы, тем самым снижая желудочную секрецию. Их действие не направлено только на холинорецепторы париетальных клеток, они блокируют М-холинорецепторы в различных системах органов. Монотерапия этими препаратами не эффективна и ограничена побочными реакциями. Избирательный М-холиноблокатор пирензепин, действующий на холинорецепторы только фундальных желёз желудка по своей антисекреторной активности не может конкурировать с блокаторами Н2-рецепторов гистамина или ИПП[20].
Значительным продвижением в терапии кислотозависимых заболеваний стало создание антисекреторных препаратов, относящихся к группе блокаторов H2-гистаминовых рецепторов. Стимуляция H2-гистаминовых рецепторов париетальной клетки гистамином является необходимым условием для последующего секретирования соляной кислоты. Блокаторы H2-рецепторов конкурентным образом ингибируют H2-рецепторы, уменьшая, таким образом, продукцию соляной кислоты.
Самыми современными кислотоснижающими препаратами являются ингибиторы протонного насоса, которые встраиваясь в Н+/К+-АТФазу, блокируют транспортировку ею протонов (ионов водорода Н+) в просвет желудка. Продолжительность эффективного антисекреторного действия ИПП определяется тем, что все «заблокированные» Н+/К+-АТФазы заменяются в клетке новыми за 72-96 часов (а половина Н+/К+-АТФаз — за 30-48 часов)[21], что заметно больше, чем время действия любого другого противоязвенного препарата.
В настоящее время разрабатывается новая серия блокаторов Н+/К+-АТФазы, так называемые антагонисты кислотного насоса (англ. acid pump antagonist), которые, в отличие от ингибиторов протонного насоса, блокируют механизм транспортировки Н+/К+-АТФазой ионов калия К+[22].
Критерии оценки антисекреторного эффекта препаратов
Оценка антисекреторного действия различных препаратов проводится с помощью суточной рН-метрии (в России для этого обычно применяется ацидогастромонитор «Гастроскан-24»[5][7][15][21]).
Для оценки антисекреторного эффекта применяют следующие критерии:
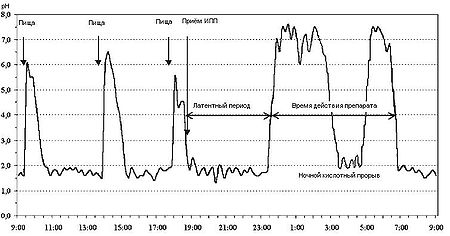
- продолжительность латентного периода — время от момента приёма препарата до того момента, когда внутрижелудочная кислотность достигнет уровня рН = 4 (этот момент считается временем начала действия препарата)[7][10][15][21];
- продолжительность времени действия препарата — время от момента начала действия, до момента, когда величина внутрижелудочного рН станет меньше 4[15] (при этом допускается, что во время периода действия рН опускается ниже 4, а затем опять поднимается) или 3[7][21];
- среднесуточное значение рН[7][10];
- процент времени с внутрижелудочным рН > 4 — характеризует выраженность времени действия[10][21];
- иногда вместо процента времени с внутрижелудочным рН > 4 рассматривают два критерия: процент времени с 4 < рН** ≤ **7** и **процент времени с рН > 7[7].
В соответствии с этими критериями установлено[7], что в отношении продолжительности времени действия, среднесуточного значения рН, процента времени с внутрижелудочным рН > 4 (а также рН > 7) ИПП превосходят блокаторы Н2-рецепторов, среди ИПП лучшие показатели в этом отношении у рабепразола[10][15]. В то же время, в отношении латентного периода такого решающего преимущества у ИПП над блокаторами Н2-рецепторов (фамотидином), нет[7].
Влияние генетических особенностей на терапию ИПП
Известно, что генетические особенности, связанные с расой, а также специфика механизма действия омепразола, лансопразола, пантопразола, эзомепразола, с одной стороны, и рабепразола, с другой, существенно влияют на ряд различий в выраженности ингибирования кислотообразования в желудке у части пациентов и, соответственно, на эффективность их лечения[23], имеется значительный разброс продолжительности антисекреторного эффекта как по разным ингибиторам протонного насоса, так и индивидуально от 1 до 12 суток[24].
Терапевтический эффект ИПП существенно зависит от скорости выведения препаратов из организма. Метаболизм всех пяти разрешенных в России ИПП происходит в печени с участием изоформ цитохрома Р450: CYP2C9, CYP2C19, CYP2D6 и CYP3A4. Полиморфизм гена, кодирующего изоформу CYR2С19, определяет различную скорость метаболизма ИПП. В российской популяции показатели распространенности мутаций гена CYP2C19 (wt/wt — гомозиготы, нет мутаций, быстрый метаболизм ИПП; wt/mt — гетерозиготы, одна мутация; mt/mt — две мутации, медленный метаболизм), кодирующего метаболизм ИПП, для представителей европеоидной расы: 50,6 %, 40,5 % и 3,3 %, для монголоидной расы — 34,0 %, 47,6 % и 18,4 %, соответственно. От 8,3 до 20,5 % пациентов резистентны к однократно принятой дозе ИПП. Полиморфизм генов системы цитохрома CYP2С19 является определяющим фактором того, что скорость наступления и длительность антисекреторного эффекта ИПП у пациентов существенно различаются.[25] Поэтому с целью исключения «неудачи» при терапии ИПП, подбор препаратов рекомендуется проводить под контролем суточной рН-метрии.[26]
Омепразоловая резистентность
В гастроэнтерологии существует понятие «омепразоловая резистентность», означающее поддержание кислотности в теле желудка ниже 4 на протяжении не менее 12 часов при суточном рН-мониторировании после двукратного приема стандартной дозы препарата. По данным В.T. Ивашкина, резистентность у взрослых к ингибиторам протонного насоса в первые сутки приема препаратов колеблется от 25,7 до 42,4 %, а на четвертые сутки — от 5,6 до 27,8 %[1].
Ночной кислотный прорыв
Ещё один феномен, связанный с применением ингибиторов протонного насоса — так называемый «ночной кислотный прорыв» — ночное понижение рН ниже 4 продолжительностью не менее часа, которое встречается у 70 % пациентов, в том числе у здоровых, вне зависимости от типа ИПП[27][28]. Впервые описан в 1998 году Peqhini P. L. c коллегами[29]. До конца причина этого феномена не ясна, но ряд авторов[27][28] объяснет его тем, что вечером, в момент приёма ИПП, не у всех пациентов все Н+/К+-АТФазы находятся в активном состоянии и ИПП не воздействует на неактивированные Н+/К+-АТФазы. Так как время выведения ИПП около часа-полутора, к моменту активации Н+/К+-АТФаз ИПП уже выведен и активированные ночью Н+/К+-АТФазы начинают секретировать соляную кислоту. Известно, что ночной кислотный прорыв никак не связан с резистентностью к некоторым ИПП.
Подбор индивидуальной терапии антисекреторными препаратами
В современной гастроэнтерологии для лечения язвенной болезни применяется около 500 препаратов[30], что косвенно показывает наличие проблемы выбора конкретного препарата (конкретной терапии) в каждом отдельном случае.
Исходя также из перечисленных выше некоторых особенностей терапии ИПП (генетика, резистентность, ночные кислотные прорывы и другое) можно утверждать, что какого-либо одного «самого современного» препарата для терапии кислотозависимых заболеваний не существует, назначение антисекреторных средств должно быть индивидуально и своевременно корректироваться с учётом реакции на проводимое лечение и, при необходимости, должно сопровождаться индивидуальным подбором препаратов и доз их приёма под контролем рН-метрии или гастроскопии[1][24].
Общие характеристики ингибиторов протонного насоса
Ингибиторы протонного насоса обладают общими для всех препаратов чертами[23]:
- похожий механизм действия, главным звеном которого является блокирование Н+/К±АТФазы;
- быстрое всасывание в двенадцатиперстной и других отделах тонкой кишки;
- неустойчивость к воздействию кислого содержимого желудка;
- высокие уровни активации в кислой среде;
- короткий период полувыведения (T1/2): не более 1 — 1,7 часа (который может быть несколько больше при почечной недостаточности);
- увеличение эффективности некоторых неустойчивых в кислой среде препаратов за счёт подъёма уровня рН в желудке;
- риск осложнений после лечения ИПП у беременных, а также у родившихся у них детей;
- врождённая или приобретённая резистентность к препаратам у части (до 10 %) пациентов;
- около 3 — 10 % пациентов имеют те или иные генетические особенности, которые сказываются на эффективности препарата, времени полувыделения, скорости метаболизма и других. важных для излечения, характеристиках.
Противопоказания и ограничения при применении ИПН
В общем противопоказаниями и ограничениями к применению ИПН являются: гиперчувствительность к замещенным бензимидазолам (фактически к ИПН), беременность (в инструкциях к некоторым препаратам содержится формулировка: допускается к применению, если польза для беременной превышает риск для матери и плода), кормление грудью, детский возраст, для некоторых ИПН — заболевания печени.[31] Конкретные противопоказания и ограничения к применению указаны в инструкциях, прилагаемых к каждому препарату.
Отсутствие в России разрешения на терапию ИПН детей раннего возраста
В Российской Федерации отсутствуют разрешения на приём ИПН детьми раннего возраста, несмотря на то, что они прошли все необходимые испытания за рубежом и применяются в развитых странах. Таким образом врач, зная об их эффективности и безопасности, не может сделать соответствующее назначение, иначе он нарушает действующие законодательные нормы.[32]
Длительный или в больших дозах приём ИПН повышает риск перелома костей
По информации FDA при приёме ИПН в течение года и дольше или в больших дозах повышается риск переломов бедра, запястья и позвоночника.[33]
Ингибиторы протонного насоса в классификаторах и перечнях
- В Анатомо-терапевтическо-химической классификации (АТХ) существует отдельная группа «Ингибиторы протонного насоса», имеющая код A02BC и входящая в раздел A02B «Противоязвенные препараты»[34]. В международном аналоге АТХ — классификаторе ATC раздел A02B называется «Препараты для лечения язвенной и гастроэзофагеальной рефлюксной болезней» (англ. Drugs for peptic ulcer and gastro-oesophageal reflux diaseas (GORD))[35].
- Группу A02BC «Ингибиторы протонного насоса» образуют следующие препараты: омепразол, пантопразол, лансопразол, рабепразол и эзомепразол.
- В АТХ также существует группа A02BD «Комбинации препаратов для эрадикации Helicobacter pylori», которая предусматривает использование омепразола, пантопразола, лансопразола и эзомепразола в составе комбинации препаратов для эрадикации Helicobacter pylori.
- Кроме входящих в группу A02BC, к ингибиторам протонного насоса относится также тенатопразол[36], новый препарат, который ещё не допущен к применению и не включён в соответствующие реестры.
- В Фармакологическим указателе также имеется отдельная группа «ингибиторы протонного насоса», которая входит в категорию «Желудочно-кишечные средства»[37].
- Один ИПП — омепразол (капсулы; лиофилизат для приготовления раствора для внутривенного введения; лиофилизат для приготовления раствора для инфузий; таблетки, покрытые оболочкой) включён в Перечень жизненно необходимых и важнейших лекарственных средств (в раздел «А02В. „Препараты для лечения язвенной болезни желудка и двенадцатиперстной кишки и гастроэзофагальной рефлюксной болезни (ГЭРБ)“»[38]).
- Стандарты медицинской помощи, утверждённые Минздравсоцразвития России, определяют, что при лечении больных:
- язвой желудка и двенадцатиперстной кишки[39] ИПП используются в 10 % случаев, гастроэзофагеальной рефлюксной болезнью[40] — в 90 %, в том числе, в 50 % из них назначается омепразол (курсовая доза 560—900 мг), в других 50 % — рабепразол (450—560 мг);
- хроническим гастритом, дуоденитом, диспепсией ИПП используются в 70 % случаев, в том числе, в 25 % из них назначается омепразол (курсовая доза 280 мг), ещё в 25 % — рабепразол (280 мг)[41];
- пищеводом Баретта ИПП используются в 80 % случаев при стационарной помощи[42] и в 100 % — при амбулаторной[43], в том числе, в 10 % из них назначается омепразол (курсовая доза 560—1200 мг), в остальных 90 % — рабепразол (при стационарной помощи; 280 мг) или эзомепразол (при амбулаторной; 2,4 г);
- с термическими и химическими ожогами пищевода — в 40 % случаев назначается омепразол (курсовая доза 400 мг), в 10 % — лансопразол (300 мг), в 10 % — эзомепразол (200 мг), в 10 % — рабепразол (200 мг)[44].
- В России разрешены к применению пять ИПП: омепразол, пантопразол, лансопразол, рабепразол и эзомепразол[31].
- Food and Drug Administration (государственный орган США) одобрены следующие 6 ИПП (указаны годы одобрения и торговые наименования лекарств во время первых регистраций): омепразол (1989, Losec), лансопразол (1995, Prevacid), рабепразол (1999, AcipHex), пантопразол (2000, Protonix), эзомепразол (2001, Nexium)[45] и декслансопразол (2009, Kapidex)[46].
Примечания
Источники
- Лопина О. Д., Котлобай А. А., Рубцов А. М. Молекулярные механизмы регуляции секреции соляной кислоты слизистой оболочки желудка. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 1997, № 6, с. 15-19.
- Бельмер С. В. и др. Медикаментозная коррекция кислотозависимых состояний. В кн. «Кислотозависимые состояния у детей». Под. ред. акад. РАМН В. А. Таболина, М.: 1999.
Ссылки
- Сайт «Функциональная гастроэнтерология». Ингибиторы протонной помпы.
См. также
 |
Ингибиторы протонного насоса на Викискладе? |
|---|
- Кислотность желудочного сока
- Париетальная клетка
- Водородно-калиевая аденозинтрифосфатаза (Н+/К±АТФаза)
- Противоязвенные препараты и препараты для лечения гастроэзофагеального рефлюкса
 Противоязвенные препараты Противоязвенные препараты |
|
|---|---|
| Препараты базисной терапии I ступени | |
| Антациды | Всасывающиеся: Кальция карбонат · Магния оксид · Натрия гидрокарбонат Невсасывающиеся: Алюминия фосфат · Алгелдрат · Алгелдрат + Магния гидроксид |
| м-Холинолитики | Системные: Атропин · Платифиллин · Метоциния йодид Селективные: Пирензепин |
| Препараты базисной терапии II ступени | |
| Блокаторы H2-гистаминовых рецепторов | Циметидин · Ранитидин · Фамотидин · Низатидин · Роксатидин |
| Ингибиторы протонного насоса | Омепразол · Пантопразол · Лансопразол · Рабепразол · Эзомепразол · Декслансопразол |
| Препараты, применяемые по специальным показаниям | |
| Цитопротекторы | Мизопростол · Сукральфат |
| Антихеликобактерные препараты | Антибиотики: Амоксициллин · Кларитромицин · Тетрациклин · Метронидазол · Тинидазол Препараты висмута: Висмута трикалия дицитрат · Ранитидина висмута цитрат |