kromatografi – Store norske leksikon (original) (raw)
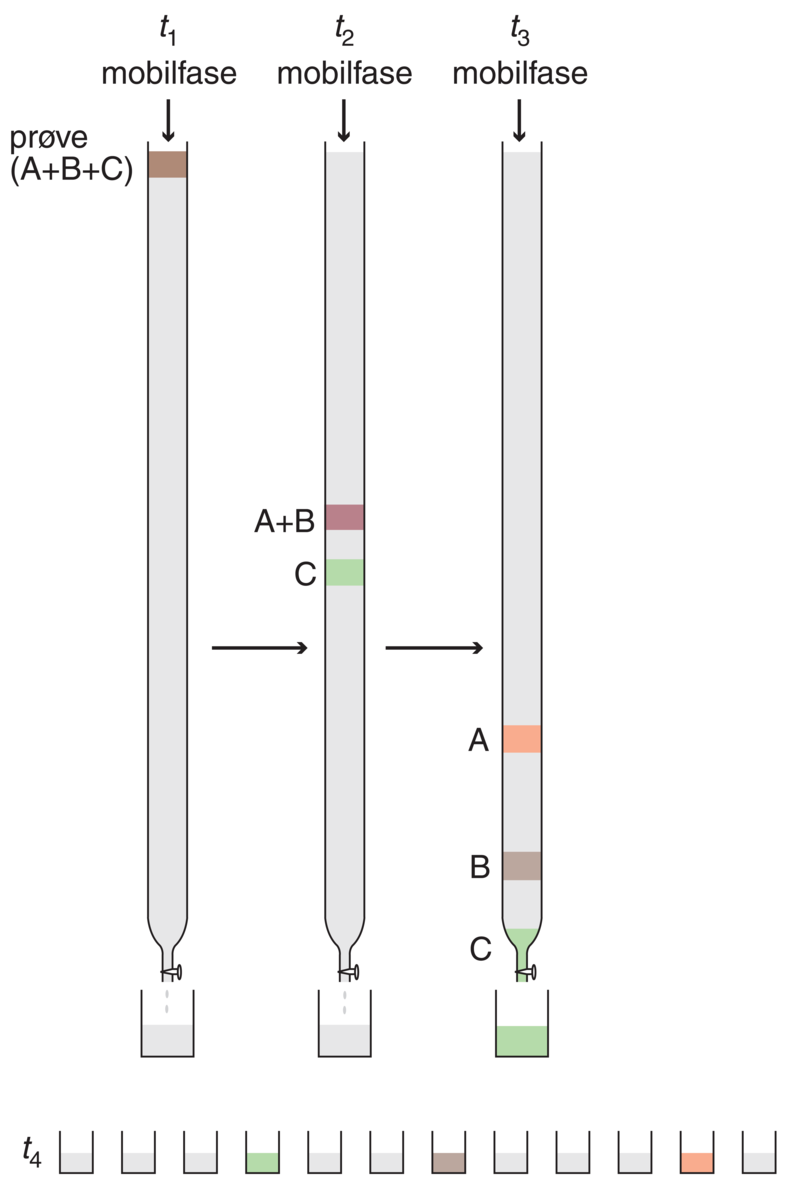
Separasjon på en kolonne med oppsamling av prøvefraksjoner. Figuren viser kolonnen, som er pakket med et fast stoff (partikler), ved forskjellige tidspunkter (t).
- t1) Prøven som inneholder stoffene A, B og C er påsatt på toppen av kolonnen. Elueringen starter når mobilfase begynner å strømme igjennom kolonnen.
- t2) Elueringen har pågått en stund, og stoffet C, som vandrer raskest gjennom kolonnen, er separert fra A og B.
- t3) Alle stoffene er separert. C er på vei ut av kolonnen og samles opp i et prøveglass.
- t4) Alle stoffene er eluert ut og samlet i fraksjoner. Noen av fraksjonene er vist i figuren.
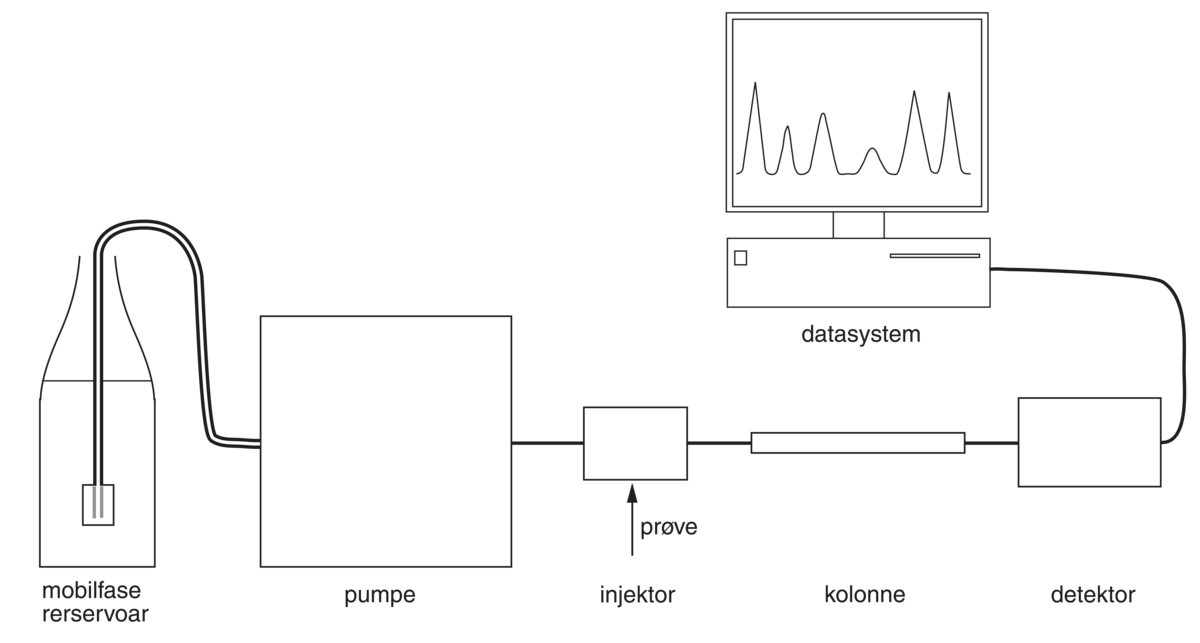
Prinsippskisse for en væskekromatograf (HPLC).
Kromatografi er metoder for separasjon av kjemiske stoffer mellom to faser, én fase som beveger seg (flytende eller gass) i en bestemt retning og én fase som står stille (fast eller gummiaktig).
Faktaboks
Uttale
kromatografˈi
Et eksempel på kromatografi er når et ark kommet bort i noe vannsøl, vann trekker inn i papiret og tusjflekker på papiret vil bli trukket bortetter sammen med vannet og separert i ulike farger. Selv om dette oftest skjer når man søler vann ved et uhell, så er det samtidig en kromatografimetode, papirkromatografi, som tidligere var mye benytta.
Kromatografi brukes ofte for å analysere en prøve for å finne ut om den inneholder et bestemt stoff, og i så fall, hvor mye av dette stoffet. Slike analyser brukes for eksempel til å bestemme mengden forurensning i en jordprøve, konsentrasjonen av et legemiddel i en blodprøve eller mengden av et forbudt stoff i en dopingprøve.
Kromatografi kan også brukes til å bestemme sammensetning av ulike stoffer i en blanding, for eksempel å bestemme andelen av metta, enumetta eller flerumetta fettsyrer i ulike typer matolje.
I noen tilfeller blir kromatografi også benytta til å separere ulike stoffer fra hverandre, for å studere hvert av de rene stoffene videre. Dette skjer på forskningslaboratorier når en blanding av stoffer inneholder noen milligram eller mikrogram av hvert enkelt stoff. Kromatografi er for upraktisk og for kostbart til å bli brukt for å separere mengder på noen få gram eller mer. Da vil andre separasjonsmetoder som for eksempel destillasjon eller utfelling brukes.
Kromatografimetoder
Det finnes en rekke ulike metoder for kromatografi. Vanlige metoder er blant annet gasskromatografi (GC), høypresisjonsvæskekromatografi (HPLC), gelkromatografi og tynnsjiktkromatografi (TLC). En metode som ble mye benytta tidligere er kolonnekromatografi, selv om metoden fremdeles benyttes av og til når man trenger relativt store mengder (0,01–10 gram) av ett eller flere stoff fra en blanding. Kolonnekromatografi er illustrert i figuren til høyre. HPLC er en forbedra form for kolonnekromatografi.
En separasjons- og analysemetode som er beslektet med kromatografi, er elektroforese. Her blir ioniske eller ioniserbare stoffer separert på grunn av forskjellig mobilitet i et elektrisk felt som settes på prøven.
Separasjonsmetoder
Alle kromatografimetoder har det til felles at stoffene som skal separeres blir fordelt mellom to ulike faser, der den ene fasen beveger seg (mobilfasen) og den andre står i ro (stasjonærfasen). Hva de to ulike fasene består av varierer. I GC er den mobile fasen en gass (hydrogen, helium eller nitrogen), mens den stasjonære fasen er en gummiaktig polymer, men av og til et fast pulver. I HPLC og TLC er den mobile fasen flytende, ofte en blanding av vann og/eller ulike organiske løsemidler, og den stasjonære fasen er som oftest i pulverform, for eksempel ikke-krystallinsk silikapulver.
Stoffene i prøven som skal separeres vil fordele seg ulikt mellom den mobile og den stasjonære fasen, og på denne måten vil stoffene i prøven bli separert fra hverandre, dersom de har ulike kjemiske egenskaper sammenligna med den mobile og den stasjonære fasen. Dette betyr også at stoffer som er veldig like kan være vanskelig å få separert fra hverandre.
I GC vil separasjonen hovedsakelig skje etter stoffenes kokepunkt, mens i TLC vil stoffene bli separert etter hva slags polaritet de har. De stoffene som har egenskaper mest lik den stasjonære fasen vil nærmest stå i ro, de stoffene som har egenskaper mest lik den mobile fasen vil bevege seg langt, og stoffer som har egenskaper delvis lik stasjonærfasen og delvis lik mobilfasen vil bevege seg middels langt. For HPLC så kan separasjonen skje som for TLC, etter polaritet, men ofte benyttes metoder som delvis separerer etter polaritet og delvis etter molekylenes størrelse og fasong.
Deteksjon og kromatogram
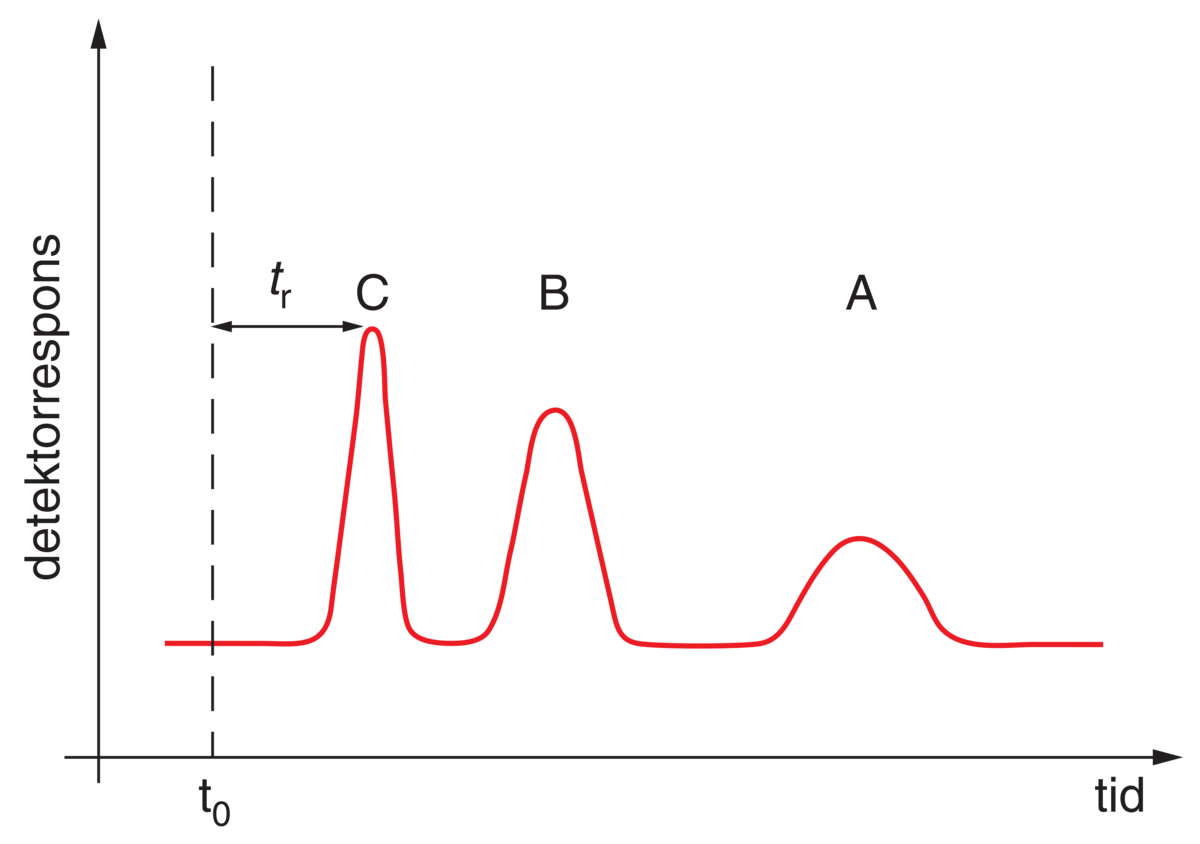
Kromatogram (detektorrespons som funksjon av tid) som fremkommer ved separasjon av stoffene A, B og C med en instrumentell metode. Retensjonstiden tr (her angitt for stoff A) er medvirkende til at man kan identifisere et stoff, og høyden eller arealet på toppen er basis for kvantitativ bestemmelse av stoffet.
Siden det er veldig små prøvemengder som blir separert, vil et GC-instrument og et HPLC-instrument alltid inkludere en detektor. For GC er flammeionisasjonsdetektoren mye brukt. Denne brenner alle stoffer etter hvert som de forlater kolonna, og ut av det som brennes blir det laga et kromatogram som viser separasjonstida (retensjonstida) i forhold til mengde stoff. Andre GC-detektorer baserer seg på for eksempel IR-spektroskopi eller massespektrometri. I parfymeindustrien benyttes også luktesansen til særskilt opptrente personer for å detektere de ulike stoffene. Disse personene sitter da og lukter på det som forlater kolonna i GC-instrumentet.
For HPLC er det vanlig å bruke en lysabsorpsjonsdetektor, men her kan man bruke for eksempel en lysspredningsdetektor eller et massespektrometer som detektor dersom stoffene som separeres ikke kan absorbere lys.
Ved å velge en detektor basert på en type spektroskopi kan man ikke bare få et kromatogram som viser separasjonstid i forhold til mengde stoff, men også spektroskopiske data samtidig, noe som hjelper til å identifisere stoffene som separeres.
Anvendelse

Et stort, moderne HPLC-instrument
GC og HPLC er de kromatografiske metodene som benyttes mest. Begge metodene kan automatiseres, slik at instrumentet kan analysere prøver døgnet rundt, hele uka. Stoffmengder som foreligger i konsentrasjonen lavere enn 10–15 g/ml (femtogram per milliliter) kan detekteres med disse metodene. Stoffer som skal analyseres med gasskromatografi må være flyktige og stabile ved den temperaturen som benyttes (som regel lavere enn 350 °C).
Et viktig bruksområde for GC er blant annet analyse av aromastoffer, oljer, gasser og alkoholer. HPLC har et større anvendelsesområde enn GC og kan også benyttes til forbindelser med høy molekylvekt og høyt kokepunkt, samt stoffer som ikke tåler oppvarming. HPLC kan for eksempel benyttes for å kontrollere medikamenter og metabolitter i blod, til å måle naturlige forekommende stoffer i kroppsvæsker og celler, til å bestemme gener, proteiner og metabolitter som er karakteristiske for arvelige sykdommer, til å bestemme næringsstoffer og giftige stoffer i matvarer, til å overvåke miljøet, til å kontrollere industrielle prosesser og måle kvaliteten av produktene.
Historikk
Det var den russiske botanikeren Mikhail Tsvet (1872–1919) som først lanserte begrepet kromatografi og som utviklet kolonnekromatografi til å separere plantepigmenter. Det har vært en enorm utvikling av kromatografien siden Tsvet introduserte teknikken i 1903, blant annet ulike instrumentelle metoder (for eksempel GC og HPLC) som kan analysere en rekke prøver etter hverandre, eller TLC og papirkromatografi som oftest er manuelle teknikker der man har mulighet til å separere mange ulike prøver samtidig, gjerne sammen med én eller flere kjente standardprøver.