Бромид ртути(I) | это... Что такое Бромид ртути(I)? (original) (raw)
| Бромид диртути(2+) | |
|---|---|
 |
|
| Систематическое название | Бромид диртути(2+) |
| Другие названия | Дибромид диртути; бромид ртути(I) |
| Химическая формула | Hg2Br2 |
| Внешний вид | твердое вещество светло-жёлтого цвета |
| Свойства | |
| Молярная масса | 560,99 г/моль |
| Температура возгонки | 345 °C (618.15 К) |
| Плотность | 7,307 г/см³ |
| Растворимость в воде | 1,5·10−6 г/100 мл |
| Произведение растворимости | 7,9·10−23 |
| Токсикологические данные | |
| ПДК | в воздухе рабочей зоны 0,2 мг/м³в атмосферном воздухе 0,0003 мг/м³в воде водоемов 0,001 мг/л |
| Структура | |
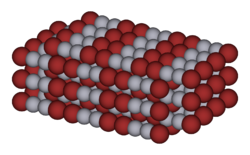
| Кристаллическая решётка | тетрагональная |
| Термодинамические свойства | |
| Стандартная энтальпия образования | −207 кДж/моль |
| Стандартная молярная энтропия | +218 Дж/(моль·К) |
| Стандартная энергия образования Гиббса | −181 кДж/моль |
| Классификация | |
| Регистрационный номер CAS | 15385-58-7 |
| Безопасность | |
| R-фразы | R26/27/28, R33, R50/53 |
| S-фразы | S13, S28, S45, S60, S61 |
Символы опасности   |
|
| Где это не указано, данные приведены при стандартных условиях (25 °C, 100 кПа). |
Броми́д дирту́ти(2+), также дибромид диртути и бромид ртути(I) — неорганическое вещество с формулой  , соединение ртути и брома. Относится к классу бинарных содинений, является солью, образованной катионом Hg22+ и анионом бромоводородной кислоты. Кристаллическое вещество светло-жёлтого цвета.
, соединение ртути и брома. Относится к классу бинарных содинений, является солью, образованной катионом Hg22+ и анионом бромоводородной кислоты. Кристаллическое вещество светло-жёлтого цвета.
Физические свойства
Бромид диртути(2+) при нормальных условиях — твёрдое вещество светло-жёлтого цвета нерастворимое в воде, этаноле, ацетоне. Возгоняется при 345 °C. Не образует кристаллогидратов.[1][2]
Имеет тетрагональную сингонию кристаллической решётки (пространственная группа I 4/mmm, a = 0,456 нм, с = 1,110 нм, Z = 2).[3]
Химические свойства
Бромид диртути(2+) не реагирует с соляной кислотой, щелочами, гидратом аммиака.
Вступает в реакции:
- с концентрированной азотной кислотой

- с горячей концентрированной серной кислотой

- с концентрированным раствором бромида калия
![\mathsf{Hg_2Br_2\ +\ 2KBr\ \longrightarrow\ K_2[HgBr_4]\ +\ Hg \downarrow}](https://dic.academic.ru/dic.nsf/ruwiki/a60cccae0e5fc64ee672edf151220032.png)
На свету медленно разлагается на бромид ртути(II) и металлическую ртуть:

Получение
Бромид диртути(2+) может быть получен:
- взаимодействием бромида ртути(II) и металлической ртути при высокой температуре [1]:

- с помощью реакций ионного обмена, например осаждением бромидом калия из раствора нитрата диртути(2+) в разбавленной азотной кислоте [1]

- анодным растворением ртути в бромомоводородной кислоте [3]
на аноде 
на катоде 
Применение
Бромид диртути(2+) применяют как компонент электролитов при рафинировании металлической ртути, для электрохимических экспериментов, для синтеза ртутьорганических соединений.[3]
Токсичность
Бромид диртути(2+) является токсичным веществом. Оказывает раздражающее действие на кожу, глаза, органы дыхания. При попадании внутрь организма главным образом поражает почки, нервную ткань и органы ЖКТ.
Является очень токсичным для водных организмов. Может оказывать долговременное вредное воздействие на водную среду.
ПДК (в пересчете на Hg) составляет: в воздухе рабочей зоны 0,2 мг/м³; в атмосферном воздухе 0,0003 мг/м³; в воде водоемов 0,001 мг/л.[3]
Примечания
- ↑ 1 2 3 Лидин Р. А., Молочко В. А., Андреева Л. Л. Реакции неорганических веществ: справочник / Под ред. Р. А. Лидина. — 2-е изд., перераб. и доп. — М.: Дрофа, 2007. — С. 203. — 637 с. — ISBN 978-5-358-01303-2
- ↑ Лидин Р.А., Андреева Л. Л., Молочко В. А. Константы неорганических веществ: справочник / Под ред. Р. А. Лидина. — 2-е изд., перераб. и доп. — М.: Дрофа, 2006. — С. 114, 606. — 685 с. — ISBN 5-7107-8085-5
- ↑ 1 2 3 4 Галогениды ртути на xumuk.ru. Архивировано из первоисточника 3 июля 2012.
| Растворимость кислот, оснований и солей в воде |
|---|
| H+ Li+ K+ Na+ NH4+ Ba2+ Ca2+ Mg2+ Sr2+ Al3+ Cr3+ Fe2+ Fe3+ Ni2+ Co2+ Mn2+ Zn2+ Ag+ Hg2+ Hg22+ Pb2+ Sn2+ Cu+ Cu2+ OH− P P P — P М Н М Н Н Н — Н Н Н Н Н — — Н Н Н Н F− P Н P P Р М Н Н М Р Н Н Н Р Р М Р Р М М Н Р Н Р Cl− P P P P Р Р Р Р Р Р Р Р Р Р Р Р Р Н Р Н М — Н Р Br− P P P P Р Р Р Р Р Р Р Р Р Р Р Р Р Н М Н М Р H Р I− P P P P Р Р Р Р Р Р ? Р — Р Р Р Р Н Н Н Н М Н — S2− P P P P — Р М Н Р — — Н — Н Н Н Н Н Н Н Н Н Н Н SO32− P P P P Р М М М Н ? ? М ? Н Н Н М Н Н Н Н ? Н ? SO42− P P P P Р Н М Р Н Р Р Р Р Р Р Р Р М — Н Н Р Р Р NO3− P P P P Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р — Р — Р Р NO2− P P P P Р Р Р Р Р ? ? ? ? Р М ? ? М ? ? ? ? ? ? PO43− P Н P P — Н Н Н Н Н Н Н Н Н Н Н Н Н Н ? Н Н Н Н CO32− М Р P P Р Н Н Н Н — — Н — Н Н — Н Н — Н — — ? — CH3COO− P Р P P Р Р Р Р Р — Р Р — Р Р Р Р Р Р М Р — Р Р CN− P Р P P Р Р Р Р Р ? Н Н — Н Н Н Н Н Р Н Р — — Н SiO32− H Н P P ? Н Н Н Н ? ? Н ? ? ? Н Н ? ? ? Н ? ? ? |
| Соединения брома |
|---|
| Бромат калия (KBrO3) • Бромат кальция (Ca(BrO3)2) • Бромат натрия (NaBrO3) • Бромат серебра (AgBrO3) • Бромат стронция (Sr(BrO3)2) • Броматы • Бромид алюминия (AlBr3) • Бромид бора(III) (BBr3) • Бромид диртути(2+) (Hg2Br2) • Бромид магния (MgBr2) • Бромид меди(I) (CuBr) • Бромид меди(II) (CuBr2) • Бромиды • Бромистая кислота (HBrO2) • Бромистоводородная кислота (HBr) • Бромная кислота (HBrO4) • Бромноватая кислота (HBrO3) • Бромноватистая кислота (HBrO) • Бромопентакарбонилрений(I) (Re(CO)5Br) • Броморганические соединения • Гипобромистая кислота (HOBr) • Диоксид брома (BrO2) • Оксид брома (Br2O) • Пербромат калия (KBrO4) • Фторид брома(I) (BrF) • Фторид брома(III) (BrF3) • Фторид брома(V) (BrF5) • Хлорид брома (BrCl) |