Тритий | это... Что такое Тритий? (original) (raw)
| Тритий | |
|---|---|
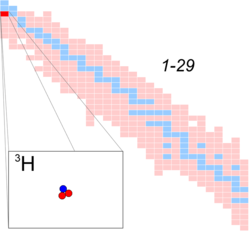 Таблица нуклидов Таблица нуклидов |
|
| Общие сведения | |
| Название, символ | Тритий, 3H |
| Альтернативные названия | сверхтяжёлый водород, T |
| Нейтронов | 2 |
| Протонов | 1 |
| Свойства нуклида | |
| Атомная масса | 3,0160492777(25)[1] а. е. м. |
| Избыток массы | 14 949,8060(23)[1] кэВ |
| Удельная энергия связи (на нуклон) | 2 827,266(1)[1] кэВ |
| Период полураспада | 12,32(2)[2] года |
| Продукты распада | 3He |
| Спин и чётность ядра | 1/2+[2] |
| Канал распада | Энергия распада |
| β− | 0,018591[1] МэВ |
Три́тий (др.-греч. τρίτος «третий»), сверхтяжёлый водород, обозначается символами T и 3H — радиоактивный изотоп водорода. Ядро трития состоит из протона и двух нейтронов, его называют тритоном и обозначают t.
В природе тритий образуется в верхних слоях атмосферы при соударении частиц космического излучения с ядрами атомов, например, азота. В процессе распада тритий превращается в 3He с испусканием электрона и антинейтрино (бета-распад), период полураспада — 12,32 года. Доступная энергия распада очень мала (18,59 кэВ), средняя энергия электронов 6,5 кэВ.
Тритий открыт английскими учёными Эрнестом Резерфордом, Маркусом Олифантом и Паулем Хартеком в 1934 году. Используется в биологии и химии как радиоактивная метка, в экспериментах по исследованию свойств нейтрино, в термоядерном оружии как источник нейтронов и одновременно термоядерное горючее, в геологии для датирования природных вод. Промышленный тритий получают облучением лития-6 нейтронами в ядерных реакторах по следующей реакции:
 .
.
Радиационная опасность трития
В силу малой энергии распада трития, испускаемые электроны хорошо задерживаются даже простейшими преградами типа одежды или резиновых хирургических перчаток. Тем не менее, этот изотоп представляет радиационную опасность при вдыхании, поглощении с пищей, впитывании через кожу. Единичный случай употребления тритиевой воды не приводит к длительному накоплению трития в организме, так как его период полувыведения — от 7 до 14 дней[3][4].
Интересные факты

Тритиевый брелок фирмы Nite
- Производство одного килограмма трития обходится в 30 млн долларов[5].
- Используется в источниках света.
Примечания
- ↑ 1 2 3 4 G. Audi, A.H. Wapstra, and C. Thibault (2003). «The AME2003 atomic mass evaluation (II). Tables, graphs, and references.». Nuclear Physics A 729: 337—676. DOI:10.1016/j.nuclphysa.2003.11.003.
- ↑ 1 2 G. Audi, O. Bersillon, J. Blachot and A. H. Wapstra (2003). «The NUBASE evaluation of nuclear and decay properties». Nuclear Physics A 729: 3–128. DOI:10.1016/j.nuclphysa.2003.11.001.
- ↑ Backgrounder on Tritium, Radiation Protection Limits, and Drinking Water Standards (англ.). U.S.NRC (февраль 2011). Архивировано из первоисточника 14 октября 2012. Проверено 5 октября 2012.
- ↑ R. V. Osborne Review of the Greenpeace report: «Tritium Hazard Report: Pollution and Radiation Risk from Canadian Nuclear Facilities» (англ.) (pdf). Canadian Nuclear Association (август 2007). Архивировано из первоисточника 14 октября 2012. Проверено 5 октября 2012.
- ↑ BBC News — Is fusion power really viable?
Ссылки
| Изотопы водорода |
|---|
| Стабильные: 1H: Протий, D, 2H: Дейтерий 10—10 000 лет: T, 3H: Тритий Нестабильные (менее суток): 4H: Водород-4, 5H: Водород-5, 6H: Водород-6, 7H: Водород-7 см. также. Водород, Таблица нуклидов |

