Муравьиная кислота | это... Что такое Муравьиная кислота? (original) (raw)
| Муравьиная кислота | |
|---|---|
 |
|
 |
|
| Общие | |
| Систематическое наименование | Метановая кислота |
| Традиционные названия | Муравьиная кислота |
| Химическая формула | HCOOH |
| Эмпирическая формула | CH2O2 |
| Физические свойства | |
| Состояние (ст. усл.) | жидкость |
| Молярная масса | 46,025380 г/моль |
| Плотность | 1,2196 г/см³ |
| Динамическая вязкость (ст. усл.) | 0,16 Па·с(при 20 °C) |
| Термические свойства | |
| Температура плавления | 8,25 °C |
| Температура кипения | 100,7 °C |
| Температура вспышки | 60 °C |
| Температура самовоспламенения | 520 °C |
| Тройная точка | 281,40 K (8,25 °C), 2,2 кПа |
| Критическая точка | 588 K (315 °C), 5,81 МПа |
| Молярная теплоёмкость (ст. усл.) | 98,74 Дж/(моль·К) |
| Энтальпия образования (ст. усл.) | −409,19 кДж/моль |
| Давление пара | 120 мм. рт. ст. (16 кПа) при 50 °C |
| Химические свойства | |
| pKa | 3,75 |
| Оптические свойства | |
| Показатель преломления | 1,3714 |
| Структура | |
| Дипольный момент | 1,41 (газ) Д |
| Классификация | |
| Рег. номер CAS | 64-18-6 |
| SMILES | O=CO |
| Регистрационный номер EC | 200-579-1 |
| RTECS | LQ4900000 |
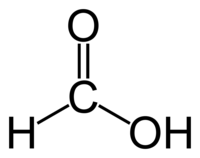
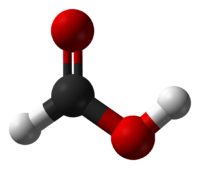
Муравьиная кислота (систематическое наименование: метановая кислота) — первый представитель в ряду насыщенных одноосновных карбоновых кислот. Зарегистрирована в качестве пищевой добавки под обозначением E236.
Формула: HCOOH
Содержание
- 1 Физические и термодинамические свойства
- 2 Получение
- 3 Безопасность
- 4 Химические свойства
- 5 Нахождение в природе
- 6 Применение
- 7 Производные муравьиной кислоты
- 8 См. также
- 9 Примечания
Физические и термодинамические свойства
При нормальных условиях муравьиная кислота представляет собой бесцветную жидкость. Растворима в ацетоне, бензоле, глицерине, толуоле. Смешивается с водой, диэтиловым эфиром, этанолом.
Свойства муравьиной кислоты
| Давление паров | 120 мм. рт. ст. (при 50 °C) |
|---|---|
| Стандартная энтальпия образования ΔH | −409,19 кДж/моль (ж) (при 298 К) |
| Стандартная энергия Гиббса образования G | −346 кДж/моль (ж) (при 298 К) |
| Стандартная энтропия образования S | 128,95 Дж/моль·K (ж) (при 298 К) |
| Стандартная мольная теплоёмкость Cp | 98,74 Дж/моль·K (ж) (при 298 К) |
| Энтальпия плавления ΔHпл | 12,72 кДж/моль |
| Энтальпия кипения ΔHкип | 22,24 кДж/моль |
| Теплота сгорания -ΔH°298 (конечные вещества CO2, H2O) | 254,58 кДж/моль |
Плотность водных растворов муравьиной кислоты при 20 °C
| Массовое содержание HCOOH, % | 1 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 22 | 26 | 30 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ρ, г/см³ | 1,0020 | 1,0045 | 1,0094 | 1,0142 | 1,0197 | 1,0247 | 1,0297 | 1,0346 | 1,0394 | 1,0442 | 1,0538 | 1,0634 | 1,0730 |
Поверхностное натяжение муравьиной кислоты
| Температура, °C | 15 | 20 | 30 |
|---|---|---|---|
| σ, Н/м | 3,813·10−2 | 3,758·10−2 | 3,648·10−2 |
Температура кипения при давлениях ниже атмосферного
| Давление, кПа (мм. рт. ст.) | 0,133(1) | 0,667(5) | 1,333(10) | 2,666(20) | 5,333(40) |
|---|---|---|---|---|---|
| Tкип, °C | −20,0 (кр.) | −5,0 (кр.) | +2,1 (кр.) | 10,3 | 24,0 |
| Давление, кПа (мм. рт. ст.) | 7,999(60) | 13,333(100) | 26,66(200) | 53,33(400) | 101,32(760) |
| Tкип, °C | 32,4 | 43,8 | 61,4 | 80,3 | 100,7 |
Интегральная теплота растворения при 25 °C
| Число молей H2O на 1 моль HCOOH | m, моль HCOOH на 1 кг H2O | -ΔHm, кДж/моль |
|---|---|---|
| 1 | 55,51 | 0,83 |
| 2 | 27,75 | 0,87 |
| 3 | 18,50 | 0,79 |
| 4 | 13,88 | 0,71 |
| 5 | 11,10 | 0,67 |
| 6 | 9,25 | 0,62 |
| 8 | 6,94 | 0,58 |
| 10 | 5,55 | 0,56 |
| 15 | 3,70 | 0,55 |
| 20 | 2,78 | 0,55 |
| 30 | 1,85 | 0,56 |
| 40 | 1,39 | 0,57 |
| 50 | 1,11 | 0,60 |
| 75 | 0,740 | 0,65 |
| 100 | 0,555 | 0,66 |
| ∞ | 0,0000 | 0,71 |
Получение
- Как побочный продукт в производстве уксусной кислоты жидкофазным окислением бутана.
- Окисление метанола:

- Реакцией монооксида углерода с гидроксидом натрия:
NaOH + CO → HCOONa → (+H2SO4, −Na2SO4) HCOOH
Это основной промышленный метод, который осуществляют в две стадии: на первой стадии монооксид углерода под давлением 0,6—0,8 МПа пропускают через нагретый до 120—130 °C гидроксид натрия; на второй стадии проводят обработку формиата натрия серной кислотой и вакуумную перегонку продукта. - Разложением глицериновых эфиров щавелевой кислоты. Для этого нагревают безводный глицерин со щавелевой кислотой, при этом отгоняется вода и образуются щавелевые эфиры. При дальнейшем нагревании эфиры разлагаются, выделяя углекислый газ, причём образуются муравьиные эфиры, которые после разложения водой дают муравьиную кислоту и глицерин.
Безопасность
Опасность муравьиной кислоты зависит от концентрации. Согласно классификации Европейского союза, концентрация до 10 % обладает раздражающим эффектом, больше 10 % — разъедающим.
При контакте с кожей 100%-ная жидкая муравьиная кислота вызывает сильные химические ожоги. Попадание даже небольшого её количества на кожу причиняет сильную боль, поражённый участок сначала белеет, как бы покрываясь инеем, потом становится похожим на воск, вокруг него появляется красная кайма. Кислота легко проникает через жировой слой кожи, поэтому промывание поражённого участка раствором соды необходимо произвести немедленно. Контакт с концентрированными парами муравьиной кислоты может привести к повреждению глаз и дыхательных путей. Случайное попадание внутрь даже разбавленных растворов вызывает явления тяжелого некротического гастроэнтерита.
Муравьиная кислота быстро перерабатывается и выводится организмом. Тем не менее, муравьиная кислота и формальдегид, образующиеся при отравлении метанолом, вызывают повреждение зрительного нерва и ведут к слепоте.
Химические свойства
Константа диссоциации: 1,772·10−4.
Муравьиная кислота, кроме кислотных свойств, проявляет также некоторые свойства альдегидов, в частности, восстановительные. При этом она окисляется до углекислого газа. Например:
2KMnO4 + 5HCOOH + 3H2SO4 → K2SO4 + 2MnSO4 + 5CO2↑ + 8H2O
При нагревании с сильными водоотнимающими средствами (H2SO4 (конц.) или P4O10) разлагается на воду и моноксид углерода:
HCOOH →(t) CO↑ + H2O
Нахождение в природе
В природе муравьиная кислота обнаружена в хвое, крапиве, фруктах, едких выделениях пчёл и муравьёв. Муравьиная кислота впервые была выделена в 1671 году английским натуралистом Джоном Рэйем из рыжих лесных муравьёв[1].
В больших количествах муравьиная кислота образуется в качестве побочного продукта при жидкофазном окислении бутана и лёгкой бензиновой фракции в производстве уксусной кислоты. Муравьиную кислоту получают также гидролизом формамида (~35 % от общего мирового производства); процесс состоит из нескольких стадий: карбонилирование метанола, взаимодействие метилформиата с безводным NH3 и последующий гидролиз образовавшегося формамида 75%-ной H2SO4. Иногда используют прямой гидролиз метилформиата (реакцию проводят в избытке воды или в присутствии третичного амина), гидратацию СО в присутствии щёлочи (кислоту выделяют из соли действием H2SO4), дегидрогенизацию СН3ОН в паровой фазе в присутствии катализаторов, содержащих Cu, а также Zr, Zn, Cr, Mn, Mg и др. (метод не имеет промышленного значения).
Применение
В основном, муравьиную кислоту используют как консервирующий и антибактериальный агент при заготовке корма. Муравьиная кислота замедляет процессы гниения и распада, поэтому сено и силос, обработанные муравьиной кислотой, дольше сохраняются. Муравьиная кислота также используется в протравном крашении шерсти, для борьбы с паразитами в пчеловодстве, как растворитель в некоторых химических реакциях, как отбеливатель при дублении кожи и др[источник не указан 1313 дней].
В лабораториях используют разложение жидкой муравьиной кислоты под действием горячей концентрированной серной кислоты, либо пропуская муравьиную кислоту над оксидом фосфора P2O5, для получения монооксида углерода. Схема реакции:
HCOOH →(t, H2SO4) H2O + CO↑
Производные муравьиной кислоты
Соли и эфиры муравьиной кислоты называют формиатами. Важнейшим производным муравьиной кислоты является формальдегид (метаналь, муравьиный альдегид).
См. также
Примечания
- ↑ Charles Earle Raven John Ray, naturalist : his life and works. — Cambridge University Press, 1986. — ISBN 0521310830
 Одноосновные предельные карбоновые кислоты Одноосновные предельные карбоновые кислоты |
|
|---|---|
| С0 | Муравьиная |
| С1 — С5 | Уксусная (С1) · Пропионовая (С2) · Масляная (С3) · Валериановая (С4) · Капроновая (С5) |
| С6 — С10 | Энантовая (С6) · Каприловая (С7) · Пеларгоновая (С8) · Каприновая (С9) · Ундециловая (С10) |
| С11 — С15 | Лауриновая (С11) · Тридекановая (С12) · Миристиновая (С13) · Пентадекановая (С14) · Пальмитиновая (С15) |
| С16 — С20 | Маргариновая (С16) · Стеариновая (С17) · Нонадекановая (С18) · Арахиновая (С19) · Генэйкозановая (С20) |
| С21 и более | Бегеновая (С21) · Трикозановая (С22) · Лигноцериновая (С23) · Пентакозановая (С24) · Церотиновая (С25) |
